Die Lungenmetastasektomie hat sich als wichtiger Baustein in der Behandlung von pulmonal metastasierten soliden Tumoren etabliert [1]. Unter günstigen Voraussetzungen kann die Operation dabei der konservativen Therapie und der Bestrahlung in der Verbesserung des Overall survivals (OS) überlegen sein (HR: 0.68; p < 0.001) [2]. Das Behandlungsziel ist die Verbesserung des Overall survival (OS) mit einer guten Lebensqualität. Dabei kann die „tumorfreie Zeit“ und die „chemotherapiefreie Zeit“ nach einer Metastasektomie genauso wie die progressionsfreie Zeit unter Systemtherapie, zum Gesamt-OS beitragen. In günstigen Fällen wird durch die Operation eine Heilung erzielt.
Mit der Entfernung von Lungenmetastasen werden die einzigen festgestellten Herde, von denen eine weitergehende hämatogene Streuung ausgehen kann, beseitigt. Die Wahrscheinlichkeit, einen wesentlichen Beitrag zur Verlängerung des OS mit der Metastasektomie beizutragen, hängt von der Histologie und zahlreichen weiteren Prognosefaktoren ab (Tab. 1). Je größer die Anzahl und je ausgeprägter einzelne negative Prognosefaktoren sind, desto geringer wird der positive Einfluss einer radikalen Lungenmetastasektomie sein. Daher kommt dem Erhalt der Lebensqualität, und dem Funktionserhalt der Lunge eine besondere Bedeutung zu.
Tab. 1: Negative Prognosefaktoren
|
Prognosefaktor |
Autor / Jahr |
|
Multiple Metastasen |
Pastorino 1997 [3], Younes 2011 [4], Petrella 2017 [1] |
|
Synchrones Auftreten der Metastasen |
Pastorino 1997 [3] |
|
Inkomplette Resektion (R1, R2) |
Pastorino 1997 [3], Baier 2015 [5], Cheung 2019 [6] |
|
Krankheitsfreies Intervall < 36 Monate, synchrone Metastasierung |
Pastorino 1997 [3], Younes 2011 [4], Cariboni 2019 [7], Meacci 2021 [8] |
|
Max. Größe der Hauptmetastase |
Younes 2011 [4], Meacci 2021 [8], Viehof 2019 [9] |
|
Intrathorakale Lymphknotenmetastasen |
Winter 2010, Petrella 2017 [1], Meacci 2021 [8] |
|
Myxofibrosarkome, Maligne periphere Nervenscheidentumoren und Ewingsarkome als aggressive Sarkomtypen |
Cariboni 2019 [7] |
|
Nicht klarzellige Histologie beim Nierenzellkarzinom |
Meacci 2021 [8] |
|
Männliches Geschlecht bei Melanomen |
Viehof 2018 [9] |
|
Erhöhtes CEA bei CRC |
Osoegawa 2016 [10] |
|
Negativer Hormonrezeptorstatus beim MammaCa |
Fan 2015 [11] |
Einschlusskriterien
Damit eine Lungenmetastasektomie für den Patienten wahrscheinlich einen Nutzen erbringt, müssen folgende Einschlusskriterien beachtet werden:
- Kontrollierter, besser komplett eradizierter/resezierter Primärtumor
- Keine unkontrollierbare weitere extrapulmonale Metastasierung
- Technisch mögliche komplette Entfernung aller Lungenmetastasen
- Ausreichende kardio-pulmonale Reserve für den geplanten Eingriff
- Keine bessere systemische Therapiealternative [6]
Bedeutung des Primärtumors für die Indikationsstellung
Es gibt wenig und nur sehr ungenaue Angaben, bei welcher Primärtumorart, wie häufig ausschließlich Lungenmetastasen vorkommen. Die nachfolgende Tabelle ist daher nur eine grobe Orientierung. Die Art des Primärtumors hat wesentlichen Einfluss auf die Chance einer kurativen Lungenmetastasektomie. So metastasieren Weichteilsarkome am häufigsten primär in die Lunge, die Lungenmetastasektomie hat hier einen hohen Stellenwert. Dagegen metastasieren Mammakarzinome am häufigsten in den Knochen. Die Lungenmetastasektomie kommt daher selten zur Anwendung, und dann nur bei einzelnen, oder ganz wenigen Herden nach Ausschluss einer extrapulmonalen Streuung (Tab. 2).
Tab. 2: Primärtumore und die Häufigkeit von Lungenmetastasen [12] [13] [14] [15]
|
Primärtumor |
Häufigkeit von Lungenmetastasen bei ED |
Häufigkeit von ausschließlich Lungenmetastasen |
|
Kolorektale Karzinome |
10–20 % |
10 % |
|
Nierenzellkarzinom |
25–30 % |
32 % aller Metastasierten |
|
Malignes Melanom |
Häufigster Metastasierungsort |
19 % aller Metastasierten |
|
Weichteilsarkome |
20–50 % |
70 % aller Metastasierten bei ED |
|
Kopf-Hals-Tumoren |
Ca. 8 % |
4,7 % aller Patienten bei ED |
|
MammaCa |
1,7 % entspricht 30,4 % der metastasierten Patientinnen |
Sehr selten |
Bildgebung
Die präoperative Bildgebung soll möglichst alle Metastasen in der Lunge detektieren. Dabei sollen auch Läsionen von 1-2 mm dargestellt werden, die durch intraoperative Palpation aufgefunden werden können. Noch kleinere Herde sind in der Regel nicht palpierbar, wenn sie nicht unmittelbaren Kontakt zur visceralen Pleura haben. Dafür eignet sich das KM-CT des Thorax in dünnen Schichten (1mm). Mittels Maximum intensity projection (MIP) lassen sich Herde besser von Gefäßstrukturen unterscheiden und die Detektion aller Metastasen wird am besten durch KI-gestützte Analyse (Computer assisted detection = CAD) ergänzt [16] [17]. Leider kann die Durchführung des Thorax-CT und PET-CT keine absolute Sicherheit für die Detektion aller Herde bieten [18].
Operativer Zugang
Die Entscheidung für das minimalinvasive oder offene Vorgehen basiert auf drei Überlegungen: ist es ein diagnostischer Eingriff, dann ist die VATS zu präferieren. Ist es eine singuläre Metastase, oder sind nicht mehr als zwei Herde im CT zu sehen, so ist ebenfalls ein minimalinvasives Vorgehen sinnvoll. Ist jedoch eine vollständige Entfernung (kurative Intention) von mehr als zwei Herden geplant, sollte ein offenes Vorgehen präferiert werden. In älteren Publikationen wird berichtet, dass durch Palpation der Lunge in 20-25 % okkulte Herde getastet werden können, die auf dem präoperativen CT nicht zu sehen waren [19]. Eine Arbeitsgruppe zur Metastasenchirurgie in der ESTS hebt hervor, dass die Palpation der Lunge die sicherste Methode ist, keinen Herd zu übersehen, dass aber bei Verwendung von KM-CTs in 1mm Schichten alle Herde dargestellt werden, die durch Palpation auffindbar wären [20]. In einem Best Evidence Report wurden unter Berücksichtigung von acht retrospektiven Studien mit 337 VATS und 485 TKT keine signifikanten Unterschiede im RFS und OS festgestellt [21]. Zusammenfassend kann man sagen, dass bei guter präoperativer Bildgebung (KM-CT in dünnen Schichten ≤ 1mm, MIP, CAD-Analyse) die VATS ein geeignetes Verfahren zur Lungenmetastasektomie darstellt, sofern alle identifizierten Herde minimalinvasiv zu erreichen sind.
Technik und Ausmaß der Lungenresektion
Die Metastasenresektion erfolgt durch halbkugelförmige Ausschneidung der Metastase unter Mitnahme von 5-10 mm gesundem Lungengewebe als Sicherheitsabstand in alle Richtungen [22]. Diese Methode kann mit dem Elektrokauter oder mit dem Laser durchgeführt werden. Durch Einsatz des Lasers wird trotz dichter Resektion um die Metastase ein ausreichender Sicherheitsabstand über die Vaporisation von Gewebe, Karbonisation und Koagulation der im Patienten verbleibenden Resektionsränder erreicht und bestmöglich Lungengewebe erhalten [23, 24, 25]. Die „Verbrennung“ von Lungengewebe am Resektionsrand sorgt für eine niedrige Rate an lokalen Rezidiven (3 %) [26].
Im Vergleich dazu liegt die Rate an lokalen Rezidiven (Abb. 1) nach atypischer Klammernahtresektion zwischen 10-20 % [6]. Bei der Resektion isolierter Lungenmetastasen kann die lokale Kontrolle durch anatomische Resektion an Stelle der atypischen Resektion verbessert werden. Dass dadurch das OS verbessert wird, konnte bisher allerdings nur in einer Studie belegt werden [27, 28, 29]. Der Nutzen der verbesserten lokalen Kontrolle wird dabei durch den negativen Einfluss weiterer Prognosefaktoren überlagert.
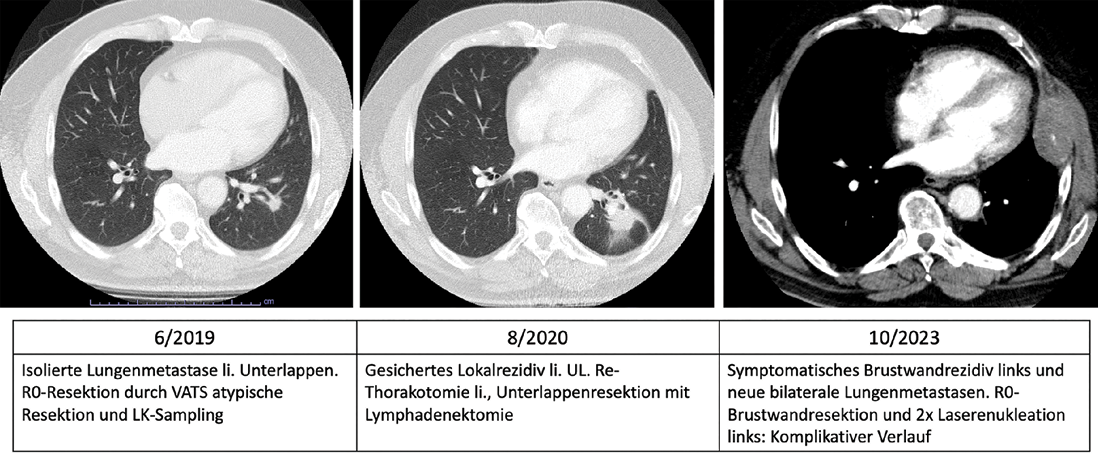
Abb. 1: Verlauf nach parenchymsparender Resektion einer isolierten kolorektalen Lungenmetastase
Lymphadenektomie
Der Befall intrathorakaler Lymphknoten kann auf zwei Hauptwegen erfolgen: durch lymphangische Ausbreitung ausgehend von Lungenmetastasen, oder aus dem Bauchraum über transdiaphragmale Lymphbahnen und den Ductus thoracicus. Letzterer Weg ist bekannt für Nierenzellkarzinome und kolorektale Lebermetastasen [30]. Die Lymphadenektomie ist Bestandteil einer kompletten Metastasenresektion. Aufgrund der unterschiedlichen Häufigkeit und prognostischen Bedeutung von Lymphknotenmetastasen bei Lungenmetastasen wird grundsätzlich ein Lymphknoten Sampling empfohlen und bei kolorektalen Karzinomen, Nierenzellkarzinomen und nicht-seminomatösen Hodentumoren auch eine systematische Lymphadenektomie [30, 31, 32]. Im Falle der intraoperativen Detektion von Lymphknotenmetastasen, soll die Metastasektomie konsequent zu Ende durchgeführt werden [31]. Auch wenn der prognostische Benefit der systematischen Lymphadenektomie bisher nicht eindeutig belegt ist, so liefert der Nachweis von intrathorakal befallenen Lymphknoten wertvolle Hinweise zur Prognose des Patienten [33].
Ergebnisse
Die Ergebnisse der Lungenmetastasenchirurgie können nach perioperativen Komplikationen, perioperative Letalität, Auftreten von Metastasenrezidiven und hinsichtlich Lebensqualität und Überleben bewertet werden. Da es bisher fast ausschließlich retrospektive Beobachtungsstudien gibt, und dabei ein erheblicher Selektionsbias besteht, sind die Aussagen mit Vorsicht zu interpretieren.
Komplikationsrate und Letalität
Die perioperative Letalität nach Lungenmetastasenresektion wird in einer Studie mit 0,1 % bei 1284 Patienten angegeben, die zwischen 2012 und 2023 operiert wurden [34]. In einer Übersichtsarbeit unter Einschluss von 61 Studien wird eine Letalität von 0 – 4,7 % nach Metastasektomie angegeben [35]. Die entsprechenden Komplikationsraten werden mit 11,3 % [34] und 0-23 % [35] angegeben. Spezifische Komplikationen nach Kauter- oder Laserenukleation sind zum einen pneumonieähnliche inflammatorische Reaktionen des Lungengewebes um die Resektionsstellen mit entsprechend radiologisch fleckförmigen Verschattungen und passager erhöhten Entzündungswerten, zum anderen prolongierte Luftfistelung, Pneumothorax und ggf. Abszess/Aspergillomentwicklung in den Resektionsdefekten. Laser assoziierte Komplikationen sind mit 6 % insgesamt selten [36].
Metastasenrezidive
Leider sind intrapulmonale Metastasenrezidive mit 38,5-42,9 % [28, 37]auch nach Resektion singulärer Metastasen, relativ häufig. Intrapulmonale Lokalrezidive an der Resektionsstelle (Abb. 1) werden mit 10,2 % – 28 % [26, 28, 29] angegeben. Der Verhinderung intrapulmonaler Lokalrezidive, insbesondere bei sonst günstigen Prognosefaktoren, kommt eine besondere Bedeutung zu. Diese kann z. B. durch anatomische Resektion, oder Laseranwendung erreicht werden [26, 28].
Gesamtüberleben
Das Gesamtüberleben (OS) und das rezidivfreie Überleben (RFS) bewegt sich in einem breiten Spektrum. So kann bei günstigen Voraussetzungen, wie z. B. bei isolierten kolorektalen Lungenmetastasen nach kompletter Resektion eine 5- und 10-Jahres Überlebensrate von 61 %-70 % und 47 % erreicht werden [4, 28], während bei ungünstiger Histologie und ungünstigen Prognosefaktoren die 5-Jahres Überlebensrate unter 25 % bleibt [4], oder gar 7 %, wenn eine komplette Metastasektomie bei Nierenzellkarzinommetastasen nicht erreicht werden konnte [5].
Diskussion
Das Auftreten ausschließlich von Lungenmetastasen ist einerseits Ausdruck der Freisetzung von zirkulierenden Tumorzellen des Primärtumors, andererseits einer gewissen Pulmotropie der Tumorzellen, wie z. B. bei den meisten Sarkomen. Diese kann erklärbar sein, wenn die Lunge die erste Filterpassage für das Blut darstellt, das als venöser Abfluss aus dem Primärtumor kommt. Zum Zeitpunkt der operativen Metastasektomie muss daher bedacht werden, dass sichtbare und okkulte Herde in der Lunge vorliegen. Die Wahrscheinlichkeit für okkulte Metastasen sinkt, je länger das krankheitsfreie Intervall und je länger eine bekannte Metastase beobachtet wurde ohne Nachweis weiterer Herde. Allerdings können Metastasen auch metastasieren, und eine lange Beobachtung von Oligometastasen, um einen schnellen Progress der metastasierten Erkrankung auszuschließen, ist daher nicht gerechtfertigt. Wenn multiple Metastasen festgestellt werden, hat es sich in der Praxis als sinnvoll erwiesen, zunächst eine Systemtherapie durchzuführen und bei stabiler, oder regredienter Erkrankung die Metastasektomie als „Residualchirurgie“ durchzuführen. Dadurch sinkt die Wahrscheinlichkeit für einen schnellen, unkontrollierbaren Krankheitsprogress. Andererseits ist bei Vorliegen weniger, nicht gesicherter Herde in der Lunge die primär vollständige Metastasektomie gerechtfertigt und bei einzelnen Entitäten kann eine Zeit der Tumornachsorge folgen. Die Systemtherapie steht dann für ein Metastasenrezidiv zur Verfügung.
Ausblick
Der zunehmende Einsatz von zielgerichteten Therapien und von Chemo-Immuntherapie führt nicht etwa dazu, dass Metastasektomien überflüssig werden, sondern eher dazu, dass Patienten auch im Stadium IV länger überleben und eine Resektion bei stabiler Metastasierungssituation angefragt wird [38]
Die Literaturliste erhalten Sie auf Anfrage via passion_chirurgie@bdc.de.

Korrespondierender Autor:
PD Dr. med. Stefan Welter
Abteilung Thoraxchirurgie
Lungenklinik Hemer

Mousa Mezher
Abteilung Thoraxchirurgie
Lungenklinik Hemer
Chirurgie
Welter S, Mezher M: Operative Therapie von Lungenmetastasen. Passion Chirurgie. 2026 April; 16(04): Artikel 03_02.