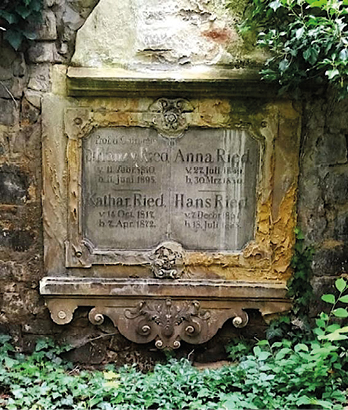Zum 215. Geburtstag
An der 1558 gegründeten Universität Jena, die 1858 ihr 300-jähriges Bestehen feiern konnte, war Franz Jordan Ried (1810–1895) Dekan der Medizinischen Fakultät und bereits seit 1846, damals als 36-jähriger Chirurg, auf den Lehrstuhl für Chirurgie berufen und zum Direktor der chirurgischen Abteilung der Landesheilanstalten, Jena, ernannt worden.
Als wir gemeinsam mit den ärztlichen Mitarbeitenden der Chirurgie im Mai 1992 zu Ehren von Prof. Dr. med. Erich Lexer [1] (1876–1973) aus Anlass seines 125. Geburtstags ein wissenschaftliches Symposium mit zahlreichen Referent:innen und Gästen (unter ihnen auch die Tochter Lexers, Frau Gunda Holzmeister), veranstalteten, da Lexer auch „Baumeister“ der neuen „Chirurgischen Universitätsklinik“ von 1910–1912 während seiner Tätigkeit in Jena bis 1919 war, stießen wir bei unseren Recherchen auf seine Vorgänger im Amt, wie z. B. Bernhard Riedel (1846–1916) und natürlich auch auf Franz Jordan von Ried (1810–1895).
Mit ihm verbinden wir in Jena den Beginn einer empirisch-wissenschaftlich orientierten regionalen und allgemeinen Chirurgie, an die man sich heute mit Hochachtung erinnert. Unsere Würdigung an dieser Stelle kann nicht sein Lebenswerk in toto wiedergeben, es ist zu umfangreich. Aber ein Kapitel seiner „lokalen Chirurgie“, nämlich sein Vorgehen bei angeborenen, kindlichen Fehlbildungen des Gesichts (speziell bei Lippen-, Kiefer- und Gaumenspalten) verdient es besonders, in die Erinnerung zurückgerufen zu werden, weil festzustellen ist, dass er damit gleichrangig in die Reihe seiner Lehrmeister (z. B.: Dieffenbach (1792–1847), Roux (1780–1854) u. a.) gehört. Bei der Betrachtung chirurgischer Techniken unserer Zeit entdeckt man auch bei v. Ried Vorläuferideen.
Mit unserem Beitrag möchten wir auf der Grundlage ausgewerteter Daten (Dissertation in Latein von E. Hoffmann [2] 1854; Dissertation von L. Koch [3] 1877; Transkription der Collegmitschrift, der zweibändigen Handschrift von E.L. Schillbach [4], 1862) den Beweis antreten, dass v. Ried methodischer Vordenker und Wegbereiter einer funktionellen Chirurgie mit hohem ästhetischem Anspruch und Orientierung am Stand der damaligen Wissenschaft war. Auch seine Würdigung 1862 als Leopoldina-Mitglied durch Friedrich Ludwig Joseph Siebert [5] (1829–1882) mit den Worten: „… war seine Meisterschaft bei der Regulierung der Hasenscharten auf das Vollendetste …“; ist ein Grund, diese „Vollendung“ näher zu betrachten.
Der am 12. Februar 1810 in Kempten im Allgäu geborene F. J. Ried besuchte in Erlangen das Gymnasium Fridericianum, nach dem Abitur 1828 studierte er in Würzburg und Erlangen Medizin. Da sein Vater bayerischer Beamter war (Landgerichts-Assessor, Stadtgerichtsrat), kam es dienstbedingt zu mehreren Ortswechseln. Im Examen musste er sich zur Anatomie des Schädels resp. des Aufbaus des Oberkiefers äußern (Marschall [7], 2005). Seine medizinische Dissertation legte er 1832 mit dem Titel: „Über den Lufteintritt in die Venen bei Chirurgischen Operationen“ vor. Danach wurde er 1833 Assistent an der Medizinischen Klinik der Universität Erlangen. 1835 legte er sein medizinisches Staatsexamen in Bamberg ab (vermutlich bei Prof. Johann Lukas Schönlein, 1793–1864; einem der Lehrer R. Virchows (1821–1902) mit Tätigkeiten in Würzburg, Jena und Bamberg). In Berlin besuchte er 1836 die Kliniken von F. v. Graefe (1787–1850), J. F. Dieffenbach (1792–1847) und lernte deren Spaltchirurgie und rekonstruktive Gesichtschirurgie kennen.
1839 folgte seine Habilitation, nachdem er sieben Kliniken in Paris (P. J. Roux, 1780–1854) und Strasbourg besucht hatte und nun ordinabel wurde. 1846 wurde Ried auf den Lehrstuhl für Chirurgie an der Universität Jena berufen. Ried (Abb. 1) kannte die französische Chirurgie und die Literatur der Operateure des 18. Jahrhunderts, zitierte z. B. F. Chopart (1743–1795) zur Cheiloplastik und war auch Zeitgenosse der deutschen Chirurgen, wie B. v. Langenbeck (1810–1887) und K. A. Burow (1809–1874), dessen Technik der Lappenplastik er anwendete und verbesserte.
Ried hatte eine sehr feine Handschrift (s. a. seine Briefe an E. Haeckel [8], 1834–1919), besaß ein ausgezeichnetes Zeichentalent und bereitete seine Eingriffe akribisch vor. Er versah seine OP- Berichte mit eigenen Skizzen, die wohl auch in seinem Colleg in seinem Privathaus an der Tafel entstanden. Ried war ein fleißiger „Kliniker“, der seine Kranken meist auch am Abend nach der Operation noch einmal aufsuchte, aber dafür weniger publizierte. Unter seiner Betreuung entstanden auch zu unserem Thema interessante medizinische Dissertationen (E. Hoffmann, 1854, L. Koch, 1877), in denen man die Beschreibung der Ideen und das Vorgehen von v. Ried findet. Lindemann [15] (1880–1970) hat 1.950 Einzelschritte, wie sie auch v. Ried anwendete, wiederholt und publiziert.

Abb. 1: Franz Jordan v. Ried (1810–1895), Fotografie des Weimarer Hoffotografen, um 1884, Sammlungen d. ThULB Jena
Eigentlich hatte sich Franz Jordan Ried Hoffnungen gemacht, in Erlangen die Nachfolge seines chirurgischen Lehrers und Freundes M. Jäger (1795–1838) antreten zu können, was aber nicht gelang, obwohl er sehr oft seinen Chef im Amt vertreten musste. In Jena begründete er mit A. Siebert (1805–1855) die „Medizinisch-Naturwissenschaftliche Gesellschaft Jena“ – auch als Ausdruck der Abkehr von der reinen naturheilkundlichen Ausrichtung der Medizin durch Hinwendung zur empirischen Wissenschaft. Er bezog die Landesheilanstalten, einen dreigeschossigen Bau ohne räumliche Trennung von septischem und aseptischem Krankengut, und erreichte die Aufteilung der Heilkunde in Chirurgie und Innere Medizin als getrennte, selbstständige Gebiete (Abb. 2).

Abb. 2: OP-Saal in den Landesheilanstalten zur Zeit F. J. Rieds. Lexer ließ mit seiner Berufung 1910 bis 1912 eine neue Chirurgische Universitäts-Klinik nach eigenen Entwürfen bauen. (Foto Arch. Chir.)
Die Stadt Jena, das Land und die Herzöge von Meiningen und Altenburg ehrten ihn in besonderer Weise (Ehrenbürger, Geheimer Rath, Ernestinischer Hausorden, was die Erhebung in den Adelsstand bedeutete). 1884 reichte er krankheitshalber nach 38-jährigem Direktorat seinen Rücktritt ein.
Franz Jordan von Ried starb am 11.06.1895 in seinem Haus in der Neugasse in Jena, nachdem ein Schlaganfall seinen rechten Arm gelähmt und sich sein Sehvermögen erheblich verschlechtert hatte. Dem Förderverein „Johannisfriedhof Jena e.V.“ (T. Peschke, 2018) [17] ist sehr zu danken, dass seine Familiengrabstelle erhalten und gepflegt wird (Abb. 3).
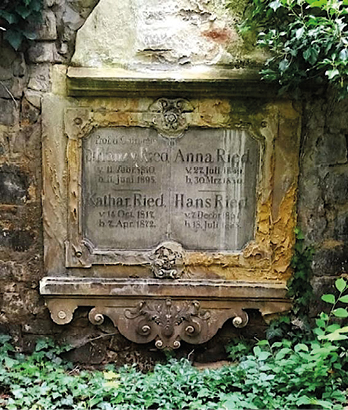
Abb. 3: Familiengrab der Familie von Ried auf dem Johannisfriedhof Jena, Foto privat
Die Spaltchirurgie ab 1846 in Jena unter Franz J. Ried
Anfänge der rein operativen Behandlung von Spaltbildungen im Mittelgesicht („Hasenscharten und Wolfsrachen“) lagen auch in Jena in der Hand von Chirurgen (Schumann, D., Rockstroh, G., Rockstroh, J. [6]).
Franz J. Ried besuchte nach seiner Promotion 1832 im Jahre 1836 auf Empfehlung seines Lehrers M. Jaeger (1795–1838) in Berlin F. v. Graefe (1787–1840), J. F. Dieffenbach und in Paris P. J. Roux. Er lernte deren Methoden zur Operation von Spaltbildungen kennen, übernahm ihr Vorgehen am Gaumen und entwickelte eigene Techniken, um Verwachsungen zwischen Gaumen und Rachen zu lösen. Während in Jena mit Ried schon 1846 eine ordentliche Professur mit Lehrstuhl für Chirurgie entstand, folgte das an „großen Universitäten“ wie z. B. in Basel fast 20 Jahre später (1864) mit Auguste Socin (1837–1899), der 27-jährig die erste Berufung eines ordentlichen Professors für Chirurgie an der Universität Basel erhielt. Bekannt sind von Socin die engen Kontakte zu den deutschen Chirurgen v. Bergmann (1836–1907), v. Langenbeck u. a.
Von F. J. Ried wurden heute modern erscheinende Schnittführungen für die Lippen-und Gaumenspalten-Operationen entworfen, die in Anlehnung an Dieffenbach und auch von seinem Zeitgenossen v. Langenbeck publiziert wurden. Insbesondere bei den bogenförmigen Inzisionen zur Chirurgie der Lippenspalten geht Ried den Verfahren heutiger populärer Methoden (z. B.: Rotation Advancement Procedure, Millard,1961 [9]) voraus. Dieses wird bei den doppelten Hasenscharten noch deutlicher (Schillbach, 1862). Auch die von uns über 20 Jahre geübte Technik nach G. Pfeifer [10] (1921–2003), 1966 publiziert als sog. „Wellenschnittverfahren“, kann man schon in dem bogenförmigen Ansatz der Inzisionen bei Ried finden. In dem Vorlesungsmanuskript von Schillbach [4] wird die von F. J. Ried geübte Methode beschrieben. Damit beginnt diese regionale Chirurgie an der chirurgischen Abteilung der Landesheilanstalten Jena und kann auf Rieds Amtsantritt 1846 datiert werden. Ried gehört u. E. damit für diese Krankheitsbilder (LKG-Spalten) in die Reihe der Protagonisten einer modernen Chirurgie in der zweiten Hälfte des 19. Jahrhunderts. Auch wenn die Veröffentlichung über seine (wohl erstmalig) durchgeführte beidseitige Oberkieferresektion unter den Chirurgen offensichtlich einen höheren Stellenwert bekommen hatte, sind die Würdigungen zu seinen Hasenscharten-Operationen durch die „Leopoldina“ bezeichnend. Damit darf zu Recht von einem Beginn der wissenschaftlichen Spaltchirurgie durch F. J. Ried in Jena ausgegangen werden.

Abb. 4: Büste F. J. v. Ried, Donndorf 1858, Kustodie (Kunstsammlung) der Universität Jena, Foto Grond
In der medizinischen Dissertation von E. Hoffmann [2] (1854) unter Ried ist dieses für die Nachwelt (in Latein) dokumentiert und erhalten. Das betrifft auch die Kenntnis und Anwendung der italienischen und indischen Methoden der Nasenrekonstruktion [16].
Handschrift von v. Ried
(im Zeugnis über Schillbach, zum Antrag auf Dozentur 1854)
E. L. Schillbach (1825–1898) war Assistent und später als a. o. Professor für Chirurgie Mitarbeiter von v. Ried.
Transkription Abb. 5: Zeugnis – Herr Dr. Schillbach hat während eines Zeitraumes von zwei Jahren als Assistent der chirurgischen Klinik fungiert. Er hat sich während dieser Zeit nicht nur durch seine Strenge, Gewissenhaftigkeit in Führung der ihm übertragenen Funktionen und durch die größte den Kranken gewidmete Sorgfalt und Humanität, sondern ganz vorzüglich durch seine dem ganzen Gebiet der Medizin und besonders der Chirurgie umfassende theoretische Kenntnisse sowie praktische Befähigung ausgezeichnet. Der unterzeichnete kann denselben unbedingt als einen seiner vorzüglichen Schüler empfehlen und hält denselben namentlich zum Dozenten der Chirurgie für befähigt. Jena, den 15. Jan. 1854. Dr. F. Ried, Direktor der chirurgischen Klinik.

Abb. 5: Handschrift von Franz J. v. Ried aus der Historischen Sondersammlung der
ThULB UNIJ (Bestand 1.64a, Dekan Martin Bl. 19–21), Foto privat
In der Collegmitschrift von Schillbach lesen wir zur „Operation der einfachen Hasenscharte“: „Die Operation sollte nun nicht nur bestehen in einer einfachen Anfrischung der Spalte („Spaltränder“). Es muss eine Verlagerung der Weichteile sattfinden. Die erste Operation besteht darin, dass man durch zwei Schnitte bis an die Wangen nur (soweit) auszuführen wie es die Lippe verlangt, man vereinigt dann die beiden oberen Läppchen, man schiebt sie aneinander, ohne (sekundäre) Wunde nach unten. Die zweite Methode: Man führt erst einen Schnitt im Halbbogen um den Nasenflügelrand. Mitte der Längsschnitte führt man einen Schnitt nach den Wangen. Reicht dieses auf einer Seite nicht, wird dieses auf der anderen Seite wiederholt. Es ist dieses für das Kind bei jeder Hasenscharte anwendbar. Das mittlere Läppchen benutzt man in Form eines Dreiecks, macht es in Bogenschnitten um die Flügel und von diesen Schnitten in die Wangen. Wesentlich ist, dass man die Teile weit ablöst, um sie recht beweglich zu machen.“
Textpassage aus der Handschrift E. L. Schillbach [4] (1862)
Transkription Abb. 6: „In früherer Zeit und historisch auch jetzt war es folgendes: man trug mit Scheren die überstehenden Ränder ab und befestigte mittels unrunder Naht (Nadel) die Ränder wieder in einer Operation. Diese Operation ist aber unzweckmäßig und zwar aus folgenden Gründen: es wird an der Seite eine Einkerbung entstehen. Bei der doppelten (Spalte) wird sich in der Mitte eine Furche bilden. Um dieses zu beheben hat man sich in neuerer Zeit viel Mühe gegeben.“ff

Abb. 6: Textpassage aus der Handschrift E. L. Schillbach [4] (1862)
Die Schriften aus der Schaffensperiode von F. J. Ried liegen in der ThULB Jena vor. Sie lassen eine Rekonstruktion seines operativen Vorgehens und einen Vergleich mit später inaugurierten, z. T. heute noch gebräuchlichen Methoden zu [14].
Das klinische Bild
Klinische Kennzeichen (Tripple D)
Defekt: offene Verbindung zwischen Mund- und Nasenhöhle (fehlender Nasenboden)
Dislokation: Fehlstellungen von Nase, Kiefer, Gaumen, Zwischenkiefer, Zahnkeimen
Deformierung: Verformung von Zwischenkiefer, Gaumenfortsätzen, Vomer Gaumensegel, Naseneingang und -scheidewand
Methode v. Ried (1862)
Transkription aus Sütterlin Handschrift (Abb. 9)
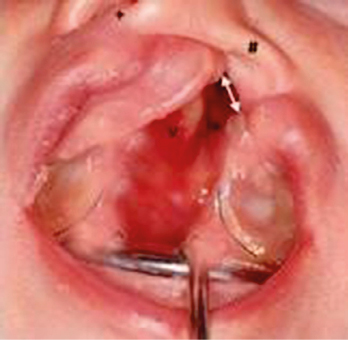
Abb. 7: Einseitig totale Spalte V – das Vomer, Foto Müller
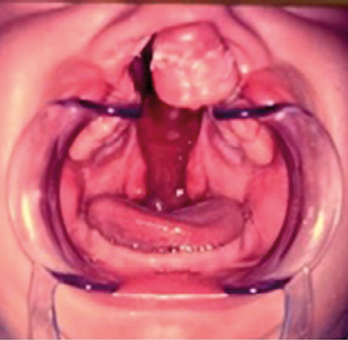
Abb. 8: Doppelseitig totale Spalte PM-Prämaxilla
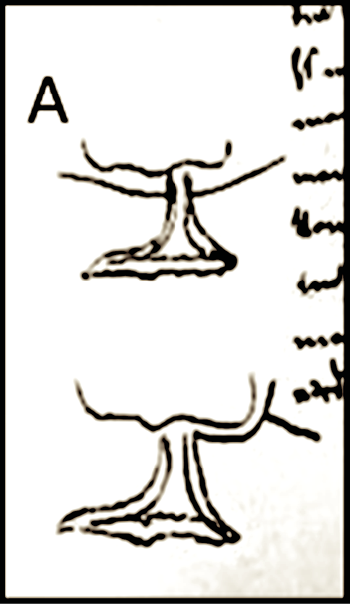

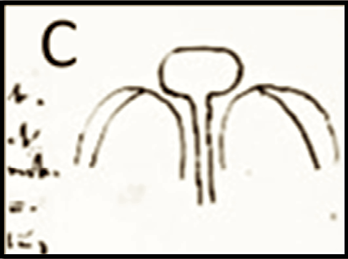
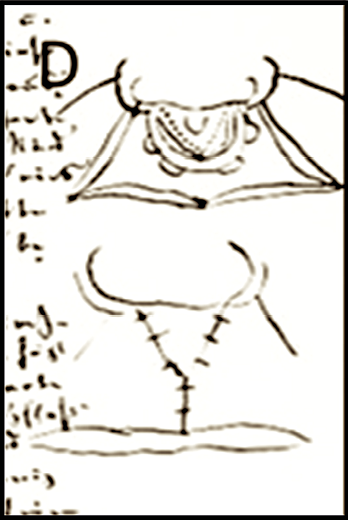
Abb. 9: Methode von Ried
„Ein erster Vorschlag ist der von Dieffenbach: er machte die Wundmachung durch zungenförmige („bogenförmige“) Schnitte. Es bleibt jedoch auch bei dieser (Methode) eine leichte Einkerbung infolge der Verkürzung der Narbe zurück. Eine weitere Methode (Ried) ist die folgende: man macht auf der einen Seite die Wundmachung vollständig, auf der anderen nur teilweise und schneidet die von unten nach oben durch. Das (entstehende) Läppchen wird herunter gebogen und vereinigt. Man (Ried) ist weiter gegangen: man hat auf beiden Seiten in dieser Weise angefrischt, so dass auf jeder Seite ein Lappen entsteht. Dasselbe Verfahren kann man auch bei der doppelten (Spalte) anwenden.“ff Seite 9
Vergleichende Betrachtung
Die Lippenplastik bei einfacher totaler „Hasenscharte“ von 1846–2005 am UNI-Klinikum Jena
V. Ried verwendete bogenförmige Inzisionen, um die verkürzten medialen Lippenanteile bei unvollständiger „Hasenscharte“ zu verlängern und dann zu vereinigen. Den Amorbogen bildete er durch ein dreieckiges Läppchen aus dem Spaltrand. Bei der OP der vollständigen „Hasenscharte“ fallen Ähnlichkeiten zu modernen Schnittführungen auf. Dies ist zwar nur ein Schritt in der Versorgung, aber wesentlich für das Endergebnis und ein Beleg für den hohen Anspruch des Vorgehens von v. Ried. Unser Vorgehen von 1972–1988 zeigt Abb. 11 und lässt Ähnlichkeiten zur Abb 12 (v. Ried) erkennen.
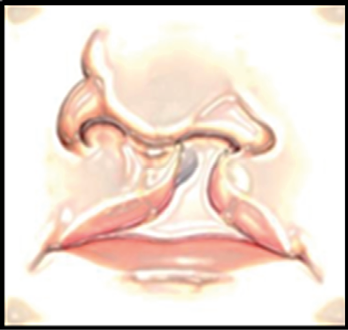
Abb. 10: Grafik li totale LKG-Spalte (Geiling)
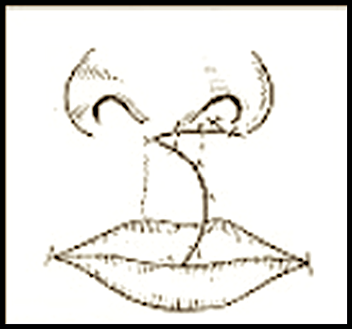
Abb. 11: Methode Millard [9]( in Jena 1972 – 1988 )
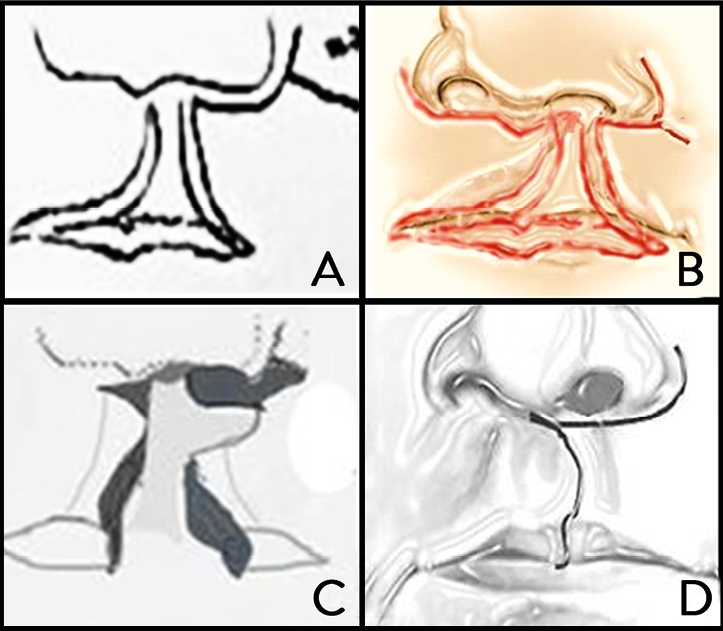
Abb. 12 A-D: Grafik zeigt die Ähnlichkeit mit der von Millard,1961 angegebenen Methode (Abb. 10 in Abb 11 (B,C) mit Umzeichnung (rot) der Lippenplastik nach v. Ried aus Schillbach, 1862)
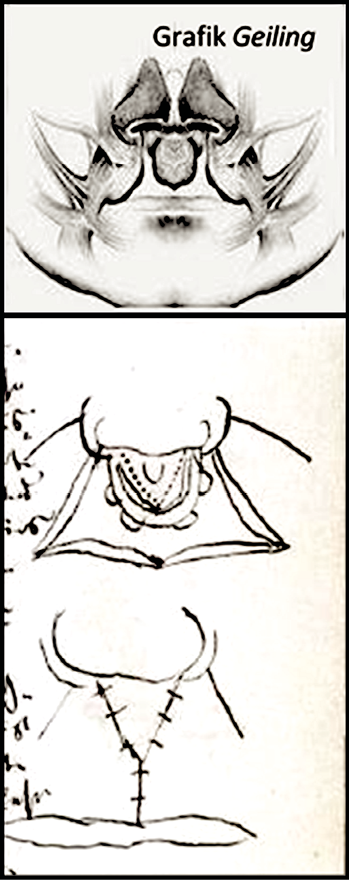
Abb. 13: Schema aus Schillbach, 1862
Die Lippenplastik bei doppelter totaler „Hasenscharte“ von 1846–2005 am UNI-Klinikum Jena
Bei den doppelten vollständigen „Hasenscharten“ hat v. Ried die Methode für die einfachen Formen auf die doppelten Spaltbildungen übertragen (Abb. 13). Es dominiert wiederum die bogenförmige Inzision mit entsprechender Ausdehnung in die Wange. Anfangs versuchte er auch den Zwischenkiefer einzuordnen, um eine regelrechte Mastikation zu erreichen.
Nach Fehlversuchen schloss er sich dem Verfahren Dieffenbachs an, der den Zwischenkiefer entfernte (Koch [3]). Auch bei der Operation der doppelseitigen LKG-Spalten hat v. Ried mit seiner Technik auch schon die Idee eines funktionell orientierten und ästhetisch anspruchsvollen Vorgehens verwirklicht.
Wir haben von 1966 an begonnen, die Millardsche Vorgehensweise anzuwenden und sind ab 1987 zur Pfeiferschen Technik mit ebenso guten Resultaten übergegangen.
Textpassage aus der Dissertation E. Hoffmann [2] (1854)
Übersetzung ‚Über die Operationen der Lippenspalte‘:
„Wir müssen zuerst definieren, was Hasenscharten sind und welche Krankheiten damit verbunden sind. Die Hasenscharte ist eine angeborene Fehlbildung, auch die Unterlippenspalte wurde einmal beobachtet. (es folgt ein Bibelspruch) Stellen wir uns nun vor, dass beispielsweise die Lippe an einem bestimmten Teil daran gehindert wird, gleichmäßig zu wachsen. Wobei der Zwischenkieferknochen beteiligt ist und sogar die Nase und Nasenlöcher verzogen und erweitert sind. Es sind Risse entstanden, jene Teile wo das Os zwischen Oberkiefer und dem Knochenteil supramaxillär sich verbindet, ist in 3 Teile geteilt. Es können doppelte Spalten vorkommen.“
E. Hoffmann, Med. Diss, Jena, 1854
Ausschnitt aus dem Text, Übersetzung aus dem Lateinischen zur „Operation der einfachen und doppelten Hasenscharte“
Zitat: „Die Operation selbst besteht darin, die Ränder, die nach und nach durch die Schleimhaut des Mundes geschützt werden, abzuschneiden und die Wunde mit blutigen Nähten zu verbinden.“
A. Operation der einfachen Lippenspalte. Akt I. Austrocknung der Ränder.
Lassen Sie uns jene Operationsmethode beschreiben, die wir mit einem Messer oder einer Schere durchführen können. Wenn Sie ein Messer verwenden möchten, greifen Sie die Lippe an der unteren Ecke der Spaltlippe entweder mit den Fingern oder einem Haken oder einer „Hakenpinzette“, wie sie es nennen, oder lassen Sie einen Partner die Lippe an der Stelle greifen, an der sich die freie Kante der Spalte befindet. Führen Sie die Lippe in den Rand der Spalte ein, ziehen Sie sie ein wenig heraus und ziehen Sie sie so heraus, sodass sie herausragt. Legen Sie dann unter den linken Teil der Lippe einen Streifen oder einen flachen Holzstreifen, in dem Sie die Lippe herausziehen und befestigen mit dem Daumen außen, mit dem Zeigefinger innen. Wenn der Streifen unter die rechte Seite der Lippe gelegt wird, wird das Messer mit der linken gegriffen und die rechte Lippe fixiert.
S. 11: Hier und da wird, wie am Anfang, mit einem Messer gearbeitet, mit einer sägeähnlichen Wirkung. Wenn Sie eine Schere verwenden, nehmen Sie die Kanten auf die bereits beschriebene Weise auf, führen Sie die scharfe Klinge der scharfen Schere mit einer kurzen, starken „Pinzette“, wie sie genannt werden, in der Nähe des Randes der Fissur bis zur oberen Naht ein und folgen Sie dabei den Verbindungen, denn es gibt welche, mit der Schere, die während der gesamten Operation von rechts geführt wird, so ist es möglich, mit einer einzigen Führungslinie mehrere Linien von der Lippe abzuschneiden, so dass keine Stelle vom Epithel verdeckt wird, ein wenig einschneiden, auf der anderen Seite das Gleiche machen und darauf achten, dass beide Seiten der Wunde gleich lang sind und in einem spitzen Winkel aufeinandertreffen. Wenn der Rand noch nicht herausgeschnitten ist, wird er mit einer Schere entnommen und entfernt. Es bleibt kein Epithel zurück, so dass eine Heilung stattfinden kann und kein Rest zurückbleiben darf. Der Blutfluss ist im Allgemeinen gering und arteriell. Dadurch können die Mundringarterien komprimiert werden, die Ligatur ist nicht gut, was immer ein Hindernis für eine schnelle Vereinigung darstellt. ff“
B. Operation der Doppellippenspalte
Dabei kommt es vor allem darauf an, ob jede Fissur gleichzeitig oder nacheinander, also erst nach vollständiger Abheilung und Kontraktion, operiert werden soll. Die meisten Chirurgen sind der ersten Meinung; andere, wie A.BELL (1837–1911, schottischer Chirurg) befürchten eine heftige Entzündung und einen Sphacelus (Gangrän) des Mittelteils, von dem ihrer Meinung nach die Zahl der Komplikationen hoch ist.
Es gibt zu viele Gründe für die „Türme“ (Bürzel-Position, Zwischenkieferstellung). Aber wenn dieser Teil groß ist, gibt es Platz für einige Nähte, wenn er kleiner ist, wird er präpariert. Was (den Zwischenkiefer) Dieffenbach immer entfernt, weil er der Meinung ist, dass der obere Teil der Oberlippe kürzer wird, insbesondere im mittleren Teil der Narbe.
Im ersten Akt wird die scharfe Klinge der Schere bis zum Nasenspalt vorgeschoben, der Rand wird breit gemacht und gleichzeitig die dünne Haut, die die Nasenlöcher verschließt, durchtrennt, so dass die Nasenlöcher gleich lang sind. Dann wird der mittlere Teil der Oberlippe von der Verbindungsstelle zur Nasenscheidewand abgetrennt, so dass der Nasenrücken dazwischen verbleibt, und der mittlere Teil wird vollständig abgeschnitten.
Damit die Teile nicht verziehen, werden alle Verbindungen zwischen der Oberlippe und dem Oberkieferknochen bis zu den Nasenlöchern gelockert. Andere möchten, dass ein größeres Stück Material übrig bleibt, das zum Nähen verwendet wird, und es ist nicht nachvollziehbar, warum es verletzt werden kann und warum nicht alles verwendet werden sollte, was man an der Lippe verwenden kann. Im Mittelteil, wenn es nicht bis zum normalen Teil der Lippe reicht, können die erneuerten Ränder, wenn sie kräftig sind, einfach mit zwei Nadeln an den restlichen Rändern der Lippe fixiert und diese zusammengefügt werden, so dass die Wunde die Form eines Y hat, was nach Meinung vieler das erfolgreichste Ergebnis hat. Die Vereinigung erfolgt wie gewohnt.“ Zitat Ende.
Bei der doppelseitigen LKG-Spalte besteht in der Dreiteilung des Oberkiefers und der Position der Prämaxilla ein chirurgisch schwer lösbares Problem, mit dem sich F. J. v. Ried auch beschäftigte. Die Med. Diss. von L. Koch [3] (1877) gibt darüber Auskunft (S. 14).

Abb. 14 aus Pfeifer (1966) Wellenschnittführung

Abb. 15
F. J. v. Ried („Operation der doppelten Hasenscharte“, Handschrift“, Schillbach, 1862)
Transkription (mit Skizze)
Seite 13: Die doppelte Hasenscharte mit doppelter Spaltung der Zwischenkieferstruktur
Das Muster (Abb. 16) ist ein seltenerer Fall, den wir schon mehrfach zu versorgen geübt haben. In früherer Zeit hat man ganz einfach die Intermaxilla mit der Schere entfernt (Dieffenbach). Es entsteht dadurch eine breite Lücke im Oberkiefer und es fehlen dann die oberen Schneidezähne. Die Lippe sinkt ein. Man hat so begonnen bis ziemlich in die heutige Zeit folgendes geübt: die rechte Nase hat man zur Aufhaltung gegebener Sicht befestigt, danach durch lange Kompression des Knochen- („Stücks“ = Prämaxilla) zurückgedrückt. Diese Maßnahme ist langdauernd, quälend und die Zähne wachsen nach rückwärts indem das („Mittel“-) Stück“ gebogen wird. Schließlich hob man den Kopf, das („Knochen“-)Stück zu brechen und zurück zu bringen. Es kann nun hier Mastikation stattfinden. Das problematische ist die Umschneidung eines dreieckigen Stücks der Wange was so eine Verbindung möglich macht, „das Teil“ in die Zahnreihe zurück zu bringen. Dieses Verfahren wird von einzelnen Chirurgen zur eigentlichen Gesichtskonstruktion (verwendet) voraus geschickt, man kann also beides zusammen machen. Die Vereinigung der Gesichtsfortsätze geschieht in analoger Weise wie bei den ersteren angegeben. Es ist dieses für das Kind bei jeder Hasenscharte anwendbar. Das mittlere Läppchen benutzt man in Form eines Dreiecks, macht es in Bogenschnitten um die Flügel und von diesen Schnitten in die Wangen. Wesentlich ist, dass man die Teile weit ablöst, um sie recht beweglich zu machen.
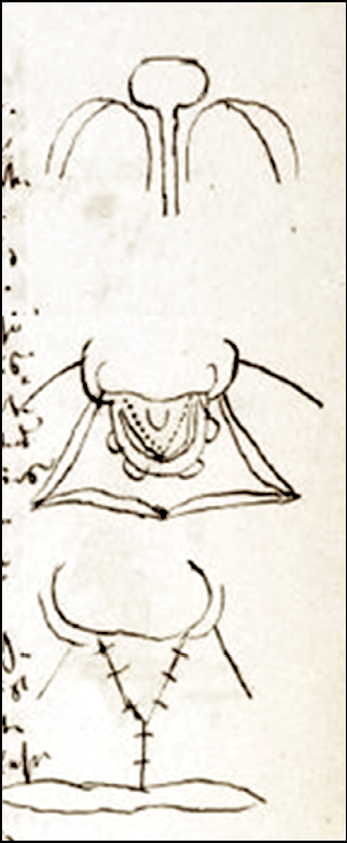
Abb. 16
Bei der Nachbehandlung ist große Vorsicht anzuraten, namentlich betreffs der Nachblutung. Blutstillende sanfte Verbandart erfolgt vom dritten, vierten Tag, dies hängt ab von der Konstitution. Früher machte man nach der Operation einen eng liierten Zuggurt daran an, heute verbindet (man) mit Streifen von Heftpflaster. Dieses war auch nötig die Nahtgefahr abzuwenden, durch einen entsprechenden Druck. Der zweckmäßigste Verband ist der Mullbindenverband. Watte oder Leinen sind bei kleinen Kindern wenig zweckmäßig. Naht ist auch gut gesichert mit Rizinusöl u. Thymianöl, in einer Menge: 1 Tropfen Rizinusöl, und 1 Tropfen Thymianöl.
Koch, L., Med. Diss., Jena, 1877 „Soll man bei der Operation der complicirten doppelseitigen Hasenschartenbildung den Zwischenkiefer erhalten oder wegnehmen“
Zusammenfassendes Postulat der Dissertation
In der von L. Koch vorgelegten Arbeit, die 1877 unter dem Ordinariat von F. J. Ried in Jena entstand, findet man das wechselvolle chirurgische Vorgehen am Zwischenkiefer beschrieben. Schon G. Dupuytren (1777–1835) hat die Erhaltung des Zwischenkiefers als mit zu viel Nachteilen behaftet eingeschätzt. J. F. Dieffenbach folgte dieser Erfahrung und resezierte die Prämaxilla mit einer Zange. B. v. Langenbeck warnte wegen der zu erwartenden Blutung vor einer „blutigen Reposition“ und versuchte anfangs die Schnittführung, die von V. v. Bruns (1812–1883) vorgeschlagen worden war, in eine Horizontale von ventral nach dorsal am Vomer zu modifizieren, um den Zwischenkiefer ohne Dislokation zurückverlagern zu können. Die frühen Ergebnisse waren anfangs akzeptabel, aber nach den späteren Kontrollen erwies sich das Vorgehen nicht dem Zweck entsprechend. Die Prämaxilla blieb beweglich und war funktionell unbrauchbar. Auch nach antiseptischem Vorgehen und unter allgemeiner Betäubung zur Schaffenszeit von F. J. v. Ried (1810–1895) sollten die Versuche der operativen Einordnung des Zwischenkiefers nicht besser werden [15].
F. J. v. Ried entfernte wie vorher o. g. Chirurgen nun in Jena bei doppelseitigen LKG-Spalten auch die Prämaxilla. Man kann feststellen, dass es nahezu bis zum Ende des 19. Jahrhunderts nicht gelang, die Bedeutung der Prämaxilla zu erkennen und dem in der Therapie Rechnung zu tragen, was natürlich operativ-technische Gründe hatte und durch Blutungen und Infektionen riskant war.

Abb. 17A: Deckblatt der Dissertation
(ThULB UNIJ )
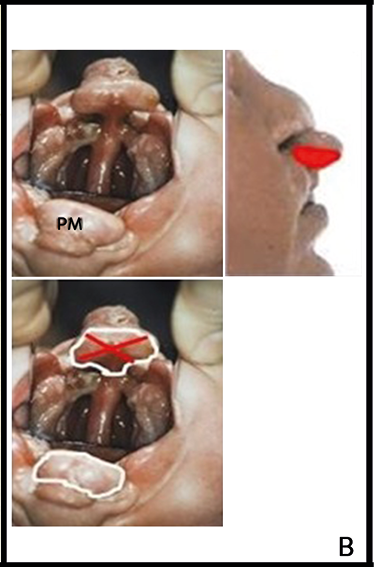
Abb. 17 B: Spiegelaufnahme (Fotos Schumann) bei doppelseitiger „komplizierter“ LKG-Spalte mit Kennzeichnung der Prämaxilla (PM rot) und der Markierung ihrer Entfernung (x)
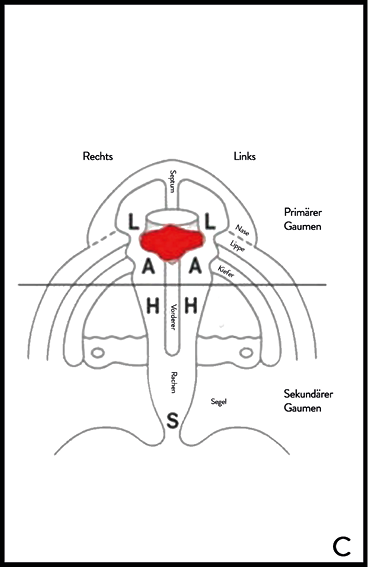
Abb. 17 C: Schema der Kennzeichnung von
Spaltbildungen des primären und sekundären
Gaumens (rot – Prämaxilla) (Dokumentationsblatt)
Zusammenfassung
Die von uns ausgewerteten Dokumente über die Schaffensperiode von F. J. v. Ried in Jena belegen bezüglich seiner geübten „regionalen Chirurgie“ von angeborenen und erworbenen Spaltbildungen des Mittelgesichts unter besonderer Berücksichtigung der LKG-Spalten einen hohen Anspruch an den Grad einer funktionellen und ästhetischen Rekonstruktion.
Aus der Vorlesungsmitschrift von Schillbach (1862) entnahmen wir Skizzen und detaillierte Beschreibungen seines Vorgehens bei ein- und doppelseitigen angeborenen Spaltbildungen, die er nach eigenen Vorstellungen und in Anlehnung an Methoden Dieffenbachs und Rouxs versorgte. Die Berücksichtigung einer angestrebten regionalen, lokalen Heilung in Verbindung mit einer Sprachverbesserung (Abschwächung der Rhinophonie), einer Unterstützung zur Entwicklung einer regelrechten Mastikation und einem hohen ästhetischen Anspruch für das Aussehen belegt die komplexe Sicht von v. Ried in seinem Therapiekonzept. Das sind Aspekte der speziellen Chirurgie angeborener, kindlicher Fehlbildungen des Gesichts, die wir bei Viktor Veau [11] (1871–1049) und Wolfgang Rosenthal [12] (1882–1971) in prinzipieller Form später wiederfinden.
Wir wollen aus Anlass der 215. Wiederkehr des Geburtstags von Franz Jordan v. Ried an seine hervorragenden Leistungen (Schröder, Trebing [13], 1997) auch auf dem Gebiet der LKG-Spalten erinnern, dem Beginn einer wissenschaftlich fundierten Spaltchirurgie in Jena mit seinem Amtsantritt 1846. Viele Anregungen haben die nachfolgenden Chirurgengenerationen durch v. Ried erhalten und die weitere Entwicklung der speziellen Chirurgie an der Universität Jena damit günstig beeinflusst, so wie auch später B. Riedel (1846–1916) und E. Lexer (1857–1937), der von 1910–1919 die Chirurgische Universitätsklinik leitete.
International agierende Teams der „Spaltchirurgie“ sind heute gut beraten, wenn sie sich auch hin und wieder mit den über 200 Jahre alten Pionierleistungen in ihrem speziellen, chirurgischen Fachgebiet beschäftigen. Das hat den Vorteil, bei neuen Konzepten „Fehler der Alten“ zu vermeiden.
Auch moderne Therapiekonzepte, bei denen der Gesamtverschluss von Lippe und Gaumen in einer Operation erfolgt (Benitez et al. [18]), legen den Fokus auf eine Heilung ohne offene Wunde, so wie es von Ried damals für die reine Lippenspalte ebenfalls wichtig und erwähnenswert fand „… man vereinigt die beiden oberen Läppchen, man schiebt sie aneinander, ohne Wunde nach unten.“
Es ist aus den Vorläufern der rein chirurgischen Behandlung eine komplexe, interdisziplinäre Therapie und Betreuung mit dem Ziel geworden, die betroffenen Kinder altersgerecht einschulen zu können. Dazu gehören Normalgehör, gut verständliche Umgangssprache, regelrechte Mastikation, sozial angepasstes Gruppenverhalten und ein unauffälliges ästhetisches Gesamtbild im Mittelgesicht.
Franz Jordan v. Ried hat uns mit seiner Vorleistung ein weniger bekanntes Lehrstück für die Chirurgie der angeborenen Fehlbildungen des kindlichen Gesichts geliefert, und das besonders für die Spaltchirurgie. Sein Beitrag für die regionale Chirurgie an der Universität Jena bleibt wohl unvergessen. Für die Unterstützung bei der Bearbeitung des Themas bedanken wir uns sehr herzlich bei Teresa Killian (ThULB) und Herrn Blankenburg, Jena.
Literatur
[1] Schumann, D., Akademische Festvorlesung zu Ehren des 125. Geburtstages von E. Lexer (1867–1937) Sonderdruck der Friedrich-Schiller – Universität Jena, 1992
[2] Hoffmann, E. Med. Diss. Jena 1854, De labii leporini operationibus
[3] Koch, L. Med. Diss. Jena 1877, Soll man bei der Operation der complicirten . doppelseitigen Hasenschartenbildung den Zwischenkiefer erhalten oder wegnehmen.
[4] Schillbach, E.L. Chirurgie Vorlesung Ried, 1862, ThULB Jena. Ms.Prov. o.45
[5] Siebert, J. Leopoldina Personalia, 1862.
[6] Schumann, D., Rockstroh, G., Rockstroh, J., Long Term Results of a Surgery – only . treatment in Patient with Cleft Lip and Palate at the surgical Clinic of the University of. Jena, Dec. 92(12), 842-47 Stomat DDR, Englisch USA.
[7] Marschall, M. Med. Diss. 2002, Die Begründung und Entwicklung des ersten . chirurgischen Lehrstuhls der Universität Jena und der chirurgischen Abteilung der . Landesheilanstalten Jena unter Franz Jordan v. Ried.[8] Taszus, Claudia (Hrsg.) 2022 Amtskorrespondenz (Ried/ Haeckel) Universität Jena. 1860–1916 Müller, Gerhard (Hrsg.)
[9] Millard R., Cleft Craft, Little Brown & Comp. Boston 1973
[10] Pfeifer, G., Lippen-Kiefer-Gaumen-Spalten, Zeitschrift f. Kinderchirurgie (Sonderdruck). 1976, 110–135
[11] Victor Veau, Bec-de-Lièvre, Hypothèse sur la Malformation initiale. Ann. d’Anat. . pathol. 1935, Jg. 12, p. 389–424.
[12] Rosenthal, Wolfgang Dtsche Zahn-, Mund- und Kieferheilkunde Bd 13,
H.1-2, 1950
[13] Schröder H., Trebing G. Bedeutende Chirurgen aus Thüringen in der 2. Hälfte des 19. Jahrhunderts Ärzteblatt Thüringen, 1997, Bd 8, S 231–234
[14] Schliephake, H., Hausamen, J-E. Lippen-, Kiefer-, Gaumen-Spalten in MKG-Chirurgie/Operationslehre, Springer 2021
[15] Lindemann, A. Die Chirurgie der Mundhöhle, der Kiefer und des Gesichts A. Barth. Leipzig 1950
[16] Joseph, J. Nasenplastik und andere Gesichtsplastiken, Curt Kabitzsch, Leipzig, 1931
[17] Peschke, T. Lebensskizzen Franz Jordan von Ried, Förderverein Johannisfriedhof Jena, e.V. 2017, Heft 17
[18] Benitez BK, Brudnicki A, Surowiec Z, Singh RK, Nalabothu P, Schumann D, Mueller AA, Kontinuierlicher zirkulärer Verschluss bei einseitiger Lippenspalte und Plattenreparatur in einer Operation, Journal of Cranio-Maxillofacial Surgery, 2022; 50(1).

Korrespondierender Autor:
Prof. em. Dr. Dr. med. Dieter A. Schumann
Facharzt für Chirurgie & Mund-Kiefer-Gesichts-Chirurgie
Burgheimer Lage 5
96049 Bamberg

Prof. Dr. med. Dr. med. dent.
Dr. phil. Andreas A. Müller
Leitung Universitäres Zentrum für Lippen-Kiefer-Gaumenspalten und Gesichtsfehlbildungen
Universitätsspital Basel
Spitalstr. 21
4031 Basel/Schweiz
Panorama
Schumann DA, Müller AA: Ein Wegbereiter der regionalen Chirurgie in Jena – Franz Jordan von Ried (1810–1895). Passion Chirurgie. 2025 Januar/Februar; 15(01/02): Artikel 09.
Panorama-Artikel finden Sie auf
BDC|Online (www.bdc.de) unter der Rubrik Wissen | Panorama.