Auch 2022, im dritten Jahr nach der großen Reform des Transplantationsgesetzes 2019, verharrten die Spenderzahlen auf niedrigem Niveau. Damit bleibt die hiesige Situation der Patientinnen und Patienten auf der Warteliste für eine Organtransplantation auch weiterhin dramatisch.
Bis Ende November 2022 gab es bundesweit 796 Organspender und Organspenderinnen in den rund 1.200 Entnahmekrankenhäusern, 7 Prozent weniger als im vergleichbaren Zeitraum des Jahres 2021. Auch die Summe der entnommenen Organe, die von Januar bis November für eine Transplantation an die internationale Vermittlungsstelle Eurotransplant gemeldet werden konnten, sank von 2.671 im Jahr 2021 auf 2.450 im Jahr 2022, was einen Rückgang um 8,3 Prozent bedeutet. Nach einem unerwarteten Einbruch der Organspendezahlen um beinahe 30 Prozent in den ersten vier Monaten 2022 fand zwar eine Stabilisierung auf dem Niveau der Vorjahre statt, doch insgesamt hat sich 2022 bis Ende November der Organmangel im Vergleich zu den Vorjahren sogar noch einmal weiter verschärft (Abb. 1 und 2).
Aus dem Eurotransplant-Verbund konnten hierzulande im vergangenen Jahr von Januar bis Ende November 2.569 Organe transplantiert werden, im Vergleichszeitraum 2021 waren es 2.740 (Abb. 3). Somit wurden in Deutschland 119 Organe mehr transplantiert als gespendet wurden, sodass wir innerhalb der Eurotransplant-Staaten, zu denen noch Belgien, Luxemburg, die Niederlande, Österreich, Kroatien, Slowenien und Ungarn gehören, weiterhin ein Importland bleiben, was Organe betrifft.
Statt der Trendwende kam Covid-19
Mit dem im April 2019 in Kraft getretenen Gesetz zur Verbesserung der Zusammenarbeit und der Strukturen bei der Organspende [4] waren zu Recht sehr viele Erwartungen verknüpft – sollte dieses doch eine Art Neustart bei der Organspende in Deutschland bewirken. Dass dabei insbesondere die klinikinternen Reformen wie z. B. die Freistellung von Transplantationsbeauftragten eine gewisse Zeit brauchen, um umgesetzt zu werden, war allen Beteiligten an der Gemeinschaftsaufgabe Organspende bewusst. Doch kaum erhofften wir uns angesichts vorsichtig steigender Organspendezahlen zu Beginn des Jahres 2020 erste Erfolge des neuen Gesetzes zu erzielen, breitete sich kurze Zeit später auch hierzulande die Coronavirus-Pandemie aus, die seitdem direkten und indirekten Einfluss auf die Arbeit in den Kliniken und damit auch die Organspende nimmt.
Erfreulicherweise kam es bei uns insbesondere zu Beginn der Pandemie nicht zu jenen massiven Einbrüchen wie in anderen europäischen Ländern, die teils Einbußen im zweistelligen Bereich verzeichnen mussten. Dank der Struktur unseres Gesundheitssystems und dem sehr engagierten Personal in den Kliniken blieben die Organspendezahlen über den Pandemieverlauf von 2020 und 2021 durchweg fast annähernd auf dem Niveau von 2019 (postmortale Organspenderinnen und Organspender Januar bis November 2019: 862; 2020: 852, 2021: 856). Jedoch führten die coronabedingten außergewöhnlichen Belastungen dann zuletzt zu Beginn des Jahres 2022 doch noch zu einem stärkeren Rückgang als erwartet.
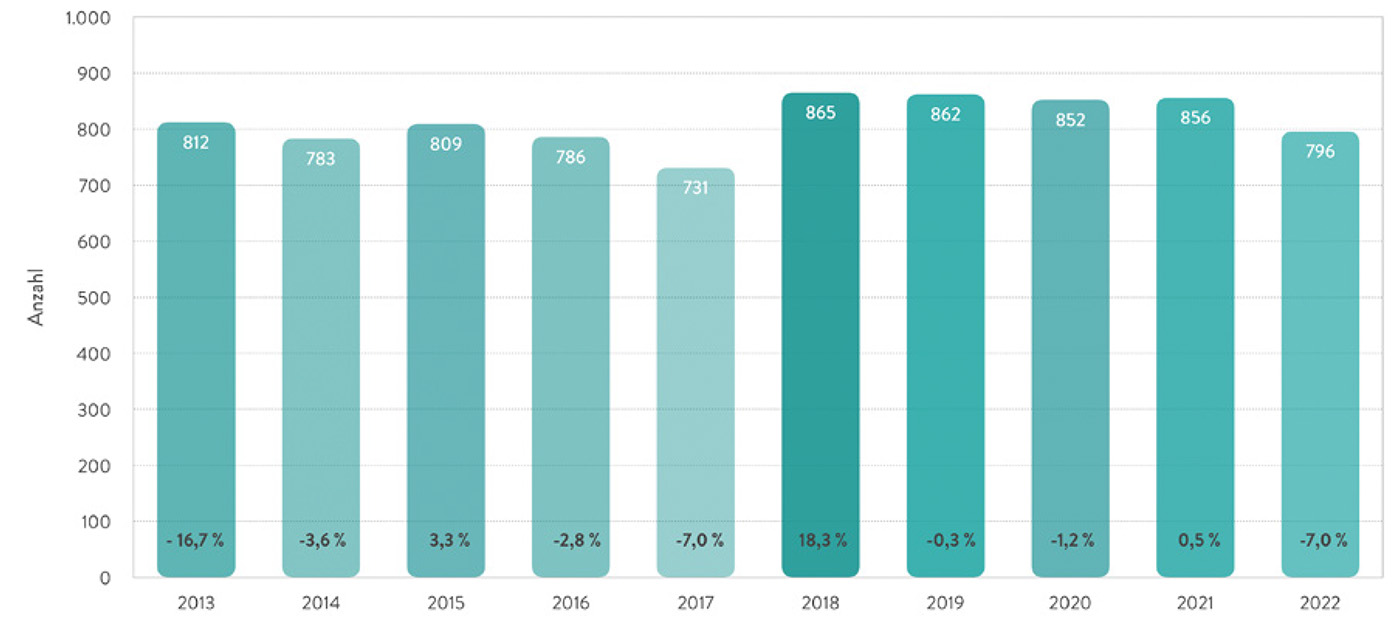
Abb. 1: Postmortale Organspender in Deutschland. Veränderung zum Vorjahr in Prozent, Januar bis November 2022* [1]
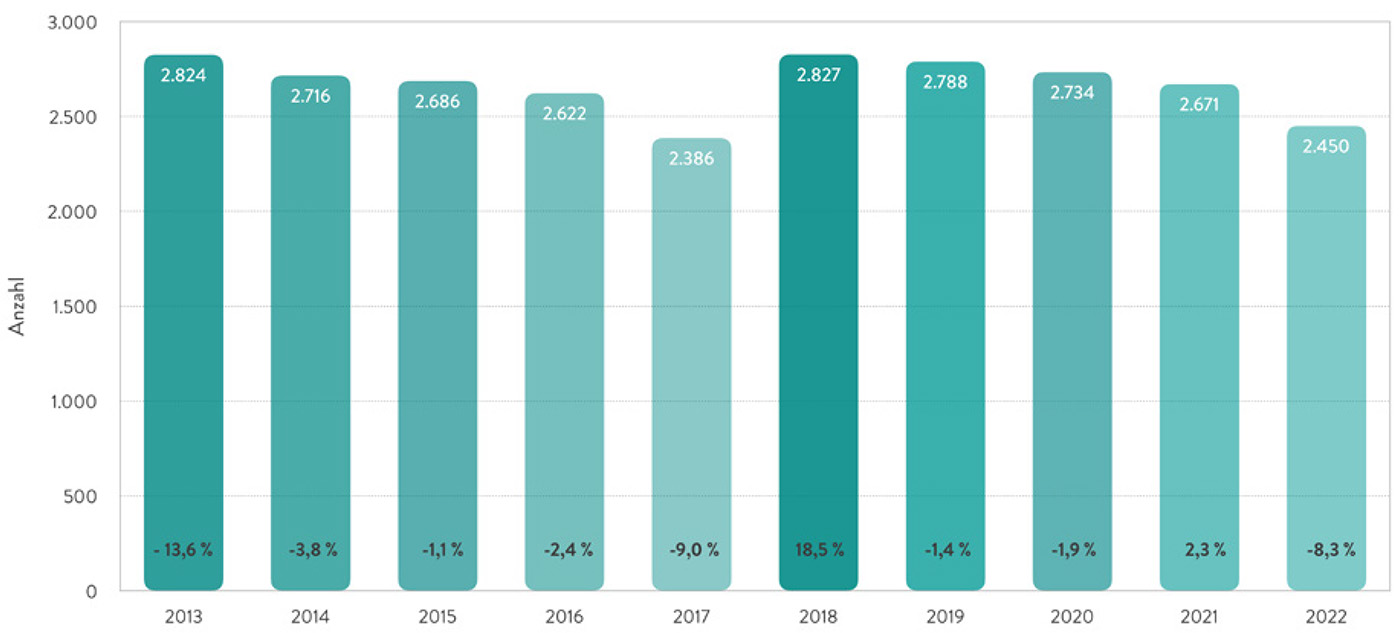
Abb. 2: Postmortal gespendete Organe in Deutschland. Veränderung zum Vorjahr in Prozent, Januar bis November 2022* [2]
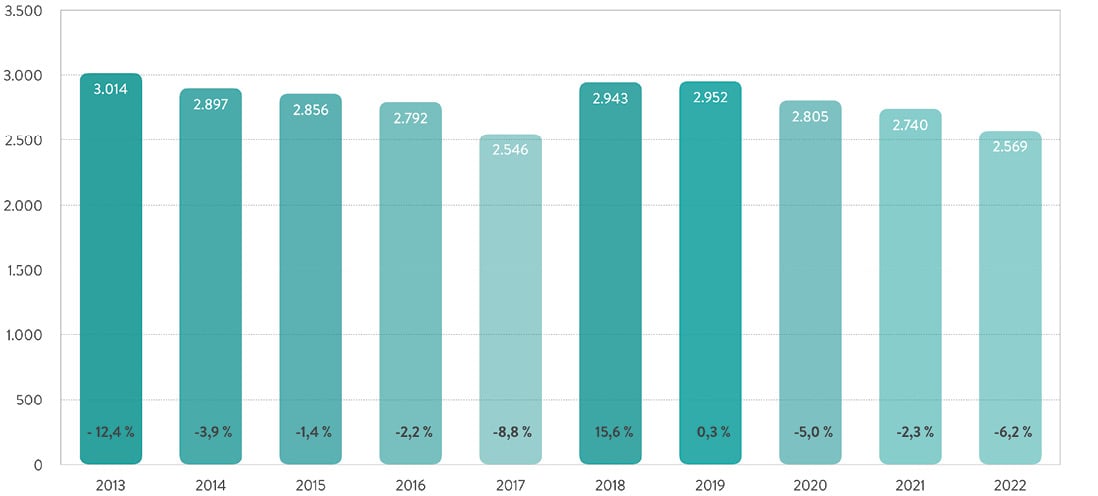
Abb. 3: Transplantierte Organe in Deutschland nach postmortaler Spende. Veränderung zum Vorjahr in Prozent, Januar bis November 2022* [3]
Denn der Jahreswechsel 2021/2022 ging mit dramatisch weniger Organspenden einher. Einer der Gründe waren in den Kliniken auch die hohen Personalausfälle, die die Omikronwelle mit sich brachte. Ein weiterer Grund: Eine nicht unerhebliche Zahl potenzieller Organspender war selbst SARS-CoV-2-positiv und wurde gemäß internationaler Empfehlungen vorsorglich von einer möglichen Spende ausgeschlossen. Erst im Verlauf des Frühjahrs 2022 wurde dies geändert, nachdem zunehmend Erfahrungen aus anderen Ländern vorlagen, die zeigten, dass bei sorgfältiger Spendercharakterisierung eine Transplantation von Organen von SARS-CoV-2-positiven Spenderinnen und Spendern vertretbar erscheint. In diesem Sinne äußerte sich auch die Bundesärztekammer in einem im Mai mit weiteren Experten veröffentlichten Positionspapier. Seitdem können nach sorgfältiger Abwägung der Risiken und Chancen auch Organe von diesen Verstorbenen vermittelt werden.
Seit Mai 2022 befinden sich die Organspendezahlen wieder auf dem Niveau der Vorjahre. Gleichzeitig hat sich die Kontaktaufnahmen der Kliniken zur DSO nochmals erhöht, ein Trend, der sich erfreulicherweise nun bereits über mehrere Jahre fortsetzt, was aber leider bislang noch nicht zu der erhofften Zunahme der Spenden geführt hat.
Auswirkungen der Pandemie auf die gesetzlichen Reformen
Viele Maßnahmen des Gesetzes aus dem Jahr 2019 konnten durch die pandemiebedingte Belastung des gesamten Gesundheitswesens nicht in dem Umfang zeitnah umgesetzt werden, wie es wünschenswert und notwendig gewesen wäre. Zudem wird eine Verschärfung des Personalmangels in vielen Kliniken berichtet. Dies macht sich insbesondere bei so komplexem Abläufen wie einer Organspende bemerkbar – sie stellen eine äußerst anspruchsvolle Aufgabe dar, die nicht nur intensivmedizinische Expertise, sondern auch Zeit und Ressourcen braucht. Gerade für kleinere Häuser ist sie ein eher seltenes Ereignis und damit eine zusätzliche Herausforderung.
Pflegerischer und ärztlicher Personalmangel sowie die fehlende Kapazität an Intensivbetten sahen die Transplantationsbeauftragten in den Entnahmekliniken dann auch als Hauptgrund für rückläufige Organspenden im ersten Quartal 2022. Dies ergab eine Online-Umfrage der DSO vom Herbst 2022, an der sich knapp 400 Transplantationsbeauftragte beteiligten [5]. Weitere Faktoren seien frühzeitige Therapielimitierungen und Ablehnungen durch Angehörige. Infektionen potenzieller Organspenderinnen und Organspender mit SARS-CoV-2 hatten hingegen laut Erhebung eine viel geringere Relevanz.
Was brachte das neue Gesetz von 2022?
Es wurde im Januar 2020 verabschiedet und trat zum 1. März 2022 in Kraft – das Gesetz zur Stärkung der Entscheidungsbereitschaft bei der Organspende [6] soll die Aufklärung der Bevölkerung über Organspende und die Willensbildung fördern. Denn letztlich können in Deutschland Organe nur dann gespendet werden, wenn eine Zustimmung dafür vorliegt.
Informiert und aufgeklärt werden sollen die Bürgerinnen und Bürger z. B. in den Ämtern, wenn sie einen neuen Pass oder Ausweis beantragen oder verlängern wollen. Die Hausärzte/-ärztinnen sollen zusätzlich alle zwei Jahre bei Bedarf ihre Patientinnen und Patienten zum Thema Organspende beraten – und ihre Entscheidung für oder gegen eine Organ- und Gewebespende soll dann in einem Online-Register dokumentiert werden können.
Bereits im Vorfeld gab und gibt es jedoch Diskussionen um Nachbesserungsbedarf. So herrscht bezüglich der Aufklärungsarbeit in den Ämtern noch Uneinigkeit über die Zuständigkeiten.
Ein anderer und für uns sehr wichtiger Punkt wurde auf unser Bestreben hin und dem der Deutschen Interdisziplinären Vereinigung für Intensiv- und Notfallmedizin (DIVI) bereits rechtzeitig zum Inkrafttreten am 1. März 2022 umgesetzt: So können die Ärztinnen und Ärzte nun bereits Einsicht in das Online-Register bekommen, wenn der irreversible Hirnfunktionsausfall unmittelbar bevorsteht oder als bereits eingetreten vermutet wird. Somit kann der Wille der Patientinnen und Patienten bezüglich einer Organspende bei Therapieentscheidungen am Ende des Lebens im Sinne der Patientenautonomie entsprechend umgesetzt werden – und diese Regelung geht auch konform mit den Vorgaben in der Richtlinie Spendererkennung der Bundesärztekammer.
Der Start des Online-Registers hat sich nun aber bereits verzögert und wird aktuell mit frühestens Ende 2023/Anfang 2024 benannt. Zudem wird es den gewünschten Erfolg nur dann bringen, wenn möglichst viele Menschen ihren Willen über die Organspende dort auch dokumentieren. Der Zugang muss daher möglichst niederschwellig sein, gleichzeitig aber den aktuellen Datenschutzbestimmungen genügen – und hier könnte eine bürokratische Hürde den gut gemeinten Ansatz zunichtemachen. Denn einen Eintrag kann man nach bisheriger Planung nur mittels Personalausweis mit Online-Ausweisfunktion vornehmen. Wer diesen noch nicht hat bzw. nicht haben möchte, wird weiterhin die Dokumentation seiner oder ihrer Entscheidung in einem Organspendeausweis oder einer Patientenverfügung vornehmen müssen
Bei der Aufklärung in den Hausarztpraxen gibt es erste Erfolge: Hier hat die Bundeszentrale für gesundheitliche Aufklärung umfangreiches Informationsmaterial bereitgestellt – zum einen zur Abgabe an die Patientinnen und Patienten, zum anderen, um das Wissen der Hausarztpraxen selber zu erhöhen. Auch die DSO bietet in ihrem E-Learning-Modul für Arztpraxen umfangreiches Info- und Lernmaterial zur Organspende an.
Ob das neue Gesetz mit den beschriebenen Maßnahmen dann tatsächlich zu einer Steigerung der Zustimmung zur Organspende in der Bevölkerung führt, werden wir allerdings frühestens in einigen Jahren sehen.
Fokus auf die Angehörigenbetreuung
Auch wenn die Situation der Organspende in den Kliniken weiterhin Grund zur Sorge gibt, hat sich zumindest einiges getan, was die Wertschätzung der Organspenderinnen und Organspender und ihrer Angehörigen betrifft. Denn mit dem Gesetz von 2019 wurden die Rahmenbedingungen für die Angehörigenbetreuung neu definiert bzw. offiziell in die Hände der DSO gelegt. Dabei haben wir die Begleitung und Unterstützung der Angehörigen schon immer als wesentlichen Bestandteil unserer Arbeit angesehen. So bieten wir den Kliniken in der Akutsituation an, dass unsere Koordinatorinnen und Koordinatoren das Angehörigengespräch zur Einwilligung in die Organspende gemeinsam mit dem behandelnden Arzt bzw. der Ärztin führt. Zudem stehen sie den Angehörigen jederzeit als Ansprechpartner im Organspendeprozess auf der Intensivstation sowie bei der Abschiednahme nach einer Organspende zur Verfügung. Auch nach Abschluss der Organspende kümmern wir uns weiterhin um die Spenderfamilien. Dazu gehören die Durchführung von Angehörigentreffen, die Information der Angehörigen über das Ergebnis der Organtransplantation in anonymisierter Form und zudem die Weiterleitung von anonymen Dankesbriefen des Organempfängers bzw. der -empfängerin an die nächsten Angehörigen sowie anonymer Antwortschreiben der nächsten Angehörigen an den Organempfänger bzw. die -empfängerin über das Transplantationszentrum, in dem das Organ übertragen wurde. Die Voraussetzung für die Weiterleitung solcher Briefe ist, dass beide Seiten ihr Einverständnis dafür erteilt haben.
Förderung der öffentlichen Wertschätzung
Die gesetzlichen Änderungen von 2019 haben den rechtlichen Rahmen für die Angehörigenbetreuung geschaffen. Um auch die gesellschaftliche Anerkennung der Organspender stärker zu fördern, hat der Gemeinschaftliche Initiativplan Organspende [7], der das verabschiedete Gesetz in der Praxis seit Sommer 2019 begleitet, den öffentlichen Dank an alle Organspenderinnen und Organspender mittels Veranstaltungen, Online-Angeboten und Gedenkstätten als eine seiner Maßnahmen aufgeführt.
Auch hier wurde bereits einiges erfolgreich umgesetzt: So fand bereits im Herbst 2019 die von der DSO organisierte erste „Zentrale Veranstaltung zum Dank an die Organspender“ im Park des Dankens, des Erinnerns und des Hoffens in Halle (Saale) statt. Bei diesem überregionalen jährlichen Treffen kommen Spenderfamilien, Organempfängerinnen und Organempfänger, Wartelistenpatientinnen und -patienten sowie Menschen aus Medizin und Politik zusammen, um der verstorbenen Organspender und -spenderinnen zu gedenken. Dieses Danken und Gedenken wird durch eine Baumpflanzaktion als Zeichen der Verbundenheit von Organspendern und -empfängern begleitet.
Aber auch in anderen Regionen Deutschlands finden mittlerweile solche öffentlichen Würdigungen für Organspender und deren Angehörige statt. So gibt es seit 2015 im Saarland die „Oasen geschenkten Lebens“ und seit 2021 das DANK-Mal auf dem Gelände der Charité Berlin, Campus Virchow, sowie eine Gedenkstätte im Patientengarten des Schwarzwald-Baar-Klinikums in Villingen-Schwenningen. Seit Herbst 2020 steht darüber hinaus die Plattform www.dankesbriefe-organspende.de als virtueller Treffpunkt für Spenderfamilien, Organempfänger, Wartelistenpatienten und alle, die sich mit den Themen Organspende und Transplantation befassen, zur Verfügung. Die Website bietet darüber hinaus praxisnahe Informationen für Transplantierte und Angehörige von Spendern zum Ablauf und den gesetzlichen Rahmenbedingungen des anonymen Briefwechsels. Betrieben wird das Portal von der DSO, mit Unterstützung der Deutschen Transplantationsgesellschaft, des Bundesverbands Niere e.V., des Bundesverbands der Organtransplantierten e. V., des Lebertransplantierten Deutschland e.V. und des Netzwerks Spenderfamilien.
DSO sorgt für Sicherheit im Organspendeprozess
Gerade in Zeiten eines eklatanten Organmangels zählt nicht nur jede Spende, sondern jedes einzelne Organ. Daher setzen wir uns als Koordinierungsstelle für die postmortale Organspende dafür ein, dass entnommene Organe in bestmöglichem Zustand an die Empfängerinnen und Empfänger weitergegeben werden. Zu diesem Zweck entwickeln und fördern wir nicht nur umfangreiche digitale Hilfsangebote für die Aufgaben der Transplantationsbeauftragten, sondern unterstützen auch neue Verfahren im Organspendeprozess. In diesem Jahr steht die Einführung der Maschinenperfusion für die Organkonservierung von Spendernieren bevor. Mit dieser Methode können Ischämieschäden gemindert und so die Funktionalität der Organe erhöht werden – was bei der wachsenden Zahl der chronischen Nierenerkrankungen samt Organbedarf dringend notwendig ist.
Bereits etabliert ist das System DSO.isys web, das aus unserer Sicht wesentlich zur Sicherheit im Organspendeprozess beiträgt und zu den vielen Unterstützungsangeboten gehört, die wir den Kliniken zur Verfügung stellen, um die Abläufe während einer Organspende zu erleichtern. Zudem erlaubt es den Transplantationszentren, schnell und effizient an Daten zu gelangen. Ein weiteres digitales Unterstützungsprogramm ist das Screeningtool DETECT, das eine frühe und systematische Spendererkennung ermöglicht. Es wurde von der Hochschulmedizin Dresden in Kooperation mit der DSO entwickelt und steht allen Kliniken kostenlos zur Verfügung. Retrospektive Todesfallanalysen in Entnahmekrankenhäusern mit DSO-TransplantCheck haben gezeigt, dass durch rechtzeitiges Erkennen mehr Spenden realisiert werden könnten. Hier kann das automatisierte elektronische Screeningtool DETECT auf den Intensivstationen einen wertvollen Beitrag leisten und die Arbeit der Transplantationsbeauftragten in den Kliniken unterstützen.
Der praxisnahe Austausch über solche Neuerungen und Optimierungen prägt unsere Zusammenarbeit mit unseren Partnern in den Kliniken. Daher haben wir dem Thema Qualitätssicherung bei der Organspende auf unserem Jahreskongress Anfang November 2022 mehrere Vorträge gewidmet, die auf der Kongress-Website auch als Video abrufbar sind: DSO Kongress 2022 Rückblick und Vorträge (z. B. Neues zu DSO.isys web, welche Untersuchungen werden zur Beurteilung thorakaler und viszeraler Organe benötigt sowie die Vorstellung von VivaScope, einem speziellen Mikroskop, das eine zeiteffiziente Unterscheidung zwischen pathologischem und gesundem Gewebe in Echtzeit ermöglicht).
Kulturwandel: dringend erforderlich
Wir sind zuversichtlich, dass sich die Lage in den Kliniken auch wieder entspannt und sich damit die 2019 gesetzlich angestoßenen Reformen zur Verbesserung der Organspende vollends entfalten können. Allerdings müssen wir mit Blick auf die rund 8.500 schwer kranken Patientinnen und Patienten auf den Wartelisten dringend über weitere grundlegende Maßnahmen nachdenken und die notwendigen gesellschaftlichen Diskussionen dazu führen. Ein wichtiger Baustein könnte hier die schon vielfach geforderte Einführung der Widerspruchslösung auch in Deutschland sein, so wie sie bereits in allen anderen Eurotransplant-Mitgliedsländern etabliert ist. Umfragen in der Bevölkerung bestätigen immer wieder eine hohe Bereitschaft zur Organspende. Eine Widerspruchsregelung könnte den Gedanken an die Organspende innerhalb der Gesellschaft und in den Kliniken weiter fördern und selbstverständlich machen und so grundlegende Voraussetzungen für einen Kulturwandel bei der Organspende schaffen.
Literatur
[1] www.dso.de/organspende/statistiken-berichte/organspende. Zugriff 19.12.22
[2] www.dso.de/organspende/statistiken-berichte/organspende. Zugriff 19.12.22
[3] www.dso.de/organspende/statistiken-berichte/organtransplantation Zugriff 19.12.22
[4] Bundesgesetzblatt im Internet. Zweites Gesetz zur Änderung des Transplantationsgesetzes – Verbesserung der Zusammenarbeit und der Strukturen bei der Organspende (2019). https://www.bundesgesundheitsministerium.de/fileadmin/Dateien/3_Downloads/Gesetze_und_Verordnungen/GuV/O/GZSO_BGBl.pdf Zugriff 19.12.22
[5] Schulze AK. Deutsche Stiftung Organtransplantation: Kultur der Organspende schaffen. Dtsch Arztebl 2022; 119(45): A-1952 / B-1623.
[6] Bundesgesetzblatt im Internet. Gesetz zur Stärkung der Entscheidungsbereitschaft bei der Organspende (2020). http://www.bgbl.de/xaver/bgbl/start.xav?startbk=Bundesanzeiger_BGBl&jumpTo=bgbl120s0497.pdf Zugriff 19.12.22
[7] Bundesministerium für Gesundheit. Gemeinschaftlicher Initiativplan Organspende (2019). https://www.bundesgesundheitsministerium.de/fileadmin/Dateien/3_Downloads/O/Organspende/Initiativplan_Organspende.pdf Zugriff 19.12.22
* Hinweis zu Abbildungen 1–3: Die kompletten Jahreszahlen zu Organspende und Transplantation inkl. Dezember 2022 lagen zum Redaktionsschluss dieser Ausgabe noch nicht vor, können aber ab Mitte Januar 2023 online hier abgerufen werden: www.dso.de/dso/presse/pressemitteilungen

Dr. med. Axel Rahmel
Medizinischer Vorstand
Deutsche Stiftung Organtransplantation
Hauptverwaltung
Deutschherrnufer 52
60594 Frankfurt am Main
Axel.Rahmel@dso.de
Panorama
Rahmel A: Organspende in Deutschland: weiterhin keine Erholung in Sicht Passion Chirurgie. 2023 Januar/Februar; 13(1/2): Artikel 09_01.
Weitere Artikel zum Thema finden Sie auf BDC|Online (www.bdc.de) unter der Rubrik Panorama.