Gelegentlich gibt es Diskussionen, ob im OP künstliche Wimpern erlaubt sind. Laut DIN 10506 (Lebensmittelhygiene – Gemeinschaftsverpflegung, 2018) sind sie im Produktionsbereich von Küchen verboten.
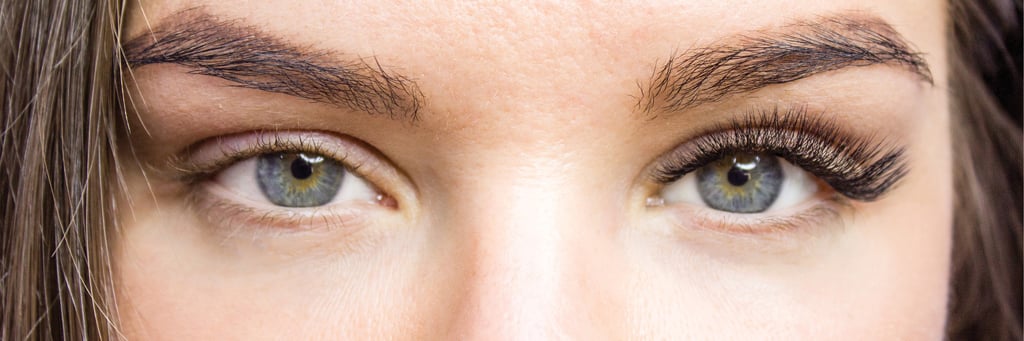
Wahrscheinlich sind nur Insidern die Spezifika künstlicher Wimpern bekannt: Es gibt zum einen Wimpernbänder, die auf die Augenlider aufgeklebt werden. Der Klebstoff dazu ist wasserlöslich, damit man die Bänder auch wieder leicht entfernen kann. Man trägt sie im allgemeinen anlassbezogen, also z. B. beim Ausgehen am Abend. Derartige künstliche Wimpern gibt es auch mit Magneten. Dabei werden die eigenen Wimpern zwischen zwei Magnetbänder eingeklemmt.
Dann gibt es Wimpern, die auf die eigenen Wimpern einzeln aufgeklebt werden. Derartige Verlängerungen gibt es auch als kleinere Büschel (Volumen-Wimpern, auch Russian Volume Look genannt), die wiederum auf dem Lid zwischen den eigenen Wimpern befestigt werden. Bei den einzelnen Wimpern-Verlängerungen werden die Wimpern-Verlängerungen mit einem dauerhaften Cyanacrylat-haltigen Kleber zu einem Drittel eingestrichen und dann auf die eigenen Wimpern (über die volle Länge) aufgegeben.
Es gibt die Wimpern in verschiedener Länge, Stärke und Form: J-Curl sind z. B. ziemlich gerade, D-Curl sind stark nach oben geschwungen (Aussehen einer Puppe). Entwickelt wurde die Technik 2003 von dem Japaner Shu Uemura. Das erste Model, bei dem er sie einsetzte, war die Sängerin Madonna. Die Kunstwimpern können aus Kunststoff sein, aber auch aus Pferde- oder Nerzhaar (Silk Lashes oder Mink Lashes).
Auch die eigenen Wimpern haben nur eine begrenzte Lebensdauer von etwa zwei bis drei Monaten, dann fallen sie aus und neue wachsen nach. Pro Tag fallen ein bis drei der echten Wimpern aus. Dies bedingt, dass die künstlichen Wimpern ca. vier Wochen auf den eigenen Wimpern bleiben und dann mit diesen verloren gehen. Man soll die künstlichen Wimpern erst auf die eigenen geben, wenn diese ausgewachsen sind (nach ca. vier Wochen). Deshalb muss man alle zwei bis drei Wochen eine Nachfüllung machen oder alle vier Wochen einen Teilersatz.
Es besteht kein Zweifel, dass künstliche ebenso wie natürliche Wimpern mit Mikroorganismen der Hautflora kontaminiert sein können. Wenn beide in den OP- Situs fallen, besteht eine Infektionsgefahr. Im Unterschied zu künstlichen Wimpern werden natürliche Wimpern wahrscheinlich abgebaut. Die zusätzliche Infektionsgefahr durch künstliche Wimpern ist jedoch nur eine theoretische Annahme, die nicht durch Studien belegt ist.
Fazit
Es gibt derzeit keine belastbaren wissenschaftlichen Untersuchungen über eine besondere Infektionsgefahr durch künstliche Wimpern. Die TRBA 250 „Biologische Arbeitsstoffe im Gesundheitswesen und in der Wohlfahrtspflege“ verbietet unter Pkt. 4.1.7. bei Tätigkeiten, die eine hygienische Händedesinfektion erfordern, das Tragen von Schmuckstücken an Händen und Unterarmen. Das Tragen von Schmuckstücken im Gesicht ist nicht genannt. Ebenso ist es in der Empfehlung zur „Prävention postoperativer Wundinfektionen“ der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (2018) formuliert.
Zumindest aus hygienischen Gründen müssen daher künstliche Wimpern im OP derzeit nicht verboten werden.
Der Kurztipp im Auftrag der DGKH gibt die Meinung der Autoren wieder.
Popp W, Pamin A, Rudke M, Meier S, Parohl N, Jatzwauk L, Kohnen W: Hygiene-Tipp: Künstliche Wimpern im OP? Passion Chirurgie. 2023 November; 13(11): Artikel 04_03.