Einleitung, Definition der chronischen Wunde
Die physiologische Wundheilung beschreibt einen mehrphasigen komplexen Prozess, in dem die physische, chemische, thermische und bakterielle Barrierefunktion der defekten Haut wiederhergestellt wird. Der Vorgang der Wundheilung durchläuft verschiedene, sich teilweise überlappende Phasen, welche durch ortsständige aktivierte Zellen und Mediatoren orchestriert und gesteuert werden. Die Hauptphasen beinhalten dabei die Exsudationsphase (auch Inflammations- oder Reinigungsphase genannt), die Granulations- oder Proliferationsphase sowie die reparative Phase oder Epithelisierungsphase, welche in der Regel nach 21 Tagen abgeschlossen sein sollte. Daran schließt sich eine längere Umbau- oder Remodellierungsphase an, die bis zu zwei Jahren andauern kann. Der ungestörte Ablauf dieser ineinander übergehenden Phasen ist entscheidend für einen erfolgreichen Wundverschluss, und Abweichungen oder Störfaktoren während einer jeder dieser Phasen können zu verzögerter oder gestörter Wundheilung und zur Entstehung von chronischen Wunden führen.
Die Definition der chronischen Wunde wird in der Literatur unterschiedlich geführt: Während für einige Autoren eine für drei oder vier Wochen oder 30 Tage bestehende Wunde als chronisch bezeichnet wird, benennen andere Autoren eine Wunde als chronisch, die nicht innerhalb von acht oder 12 Wochen beziehungsweise drei Monaten durch regelrechte Reepithelisierung geheilt ist. Daher wird auch oft ab vier Wochen der Begriff „komplizierte Wunde“ verwendet, und eine Wunde, die bei optimaler Therapie nach vier bis zwölf Wochen keine Heilungstendenz zeigt, erst nach drei Monaten als chronische Wunde bezeichnet. Jedoch gibt es bestimmte Wunden, welche nach Definition der „Initiative Chronische Wunden“ (ICW) bereits ab Entstehung als chronische Wunden einzuschätzen sind: Dazu zählen das Ulcus cruris venosum bei der chronisch-venösen Insuffizienz, der Dekubitus bei immobilen Patienten sowie Wunden bei einem diabetischen Fußsyndrom bei Diabetes mellitus.
Physiologie und Pathophysiologie der Wundheilung
Die Initialphase der Wundheilung beginnt mit der Hemostase, welche durch verletzte Kapillargefäße initiiert wird: Über das verletzte Endothelium und die dadurch freiliegende Basalmembran werden Blutplättchen aktiviert und Blutbestandteile freigesetzt. Neben der Aktivierung der Gerinnungskaskade werden auch Wachstumsfaktoren freigesetzt, welche eine Ablagerung extrazellulärer Matrix (Transforming Growth Factor-beta = TGF-beta), Chemotaxis (Platelet-derived Growth Factor = PDGF, Epidermal Growth Factor = EGF) und eine Angiogenese (Vascular Endothelial Growth Factor = VEGF) induzieren. Teilweise überlappend mit der Initialphase schließt sich die Inflammationsphase oder Exsudationsphase an, welche vom ersten bis dritten Tag andauert und sich durch eine Zellaktivierung von Leukozyten, vornehmlich Granulozyten, Neutrophilen und Monozyten, aber auch Fibroblasten und Endothelzellen auszeichnet.
Die Inflammationsphase ist wesentlich für die Vorbereitung des Wundgrundes, damit sich nachfolgend die Proliferations- oder Granulationsphase anschließen kann. Die Aktivierung der Neutrophilen ist von Tag zwei bis fünf am ausgeprägtesten und wird ab Tag drei von den Macrophagen abgelöst. Neutrophile generieren über den Weg der Myeloperoxidase freie Radikale, um Bakterien zu zerstören. Sie sezernieren proteolytische Enzyme wie Proteasen (Serum-Proteasen, Matrix-Metalloproteinasen), welche nichtvitales Gewebe aufbrechen und zersetzen. Schließlich sind die Neutrophilen in der Lage, tote Bakterien und Debris zu phagozytieren, bevor sie sich durch Apoptose selber zersetzen. Zusätzlich helfen Macrophagen, welche sich aus einwandernden Monozyten umwandeln, bei der Beseitigung von nicht-mehr funktionalen Zellen und setzen darüber hinaus weitere Wachstumsfaktoren, Chemokine und Zytokine wie TGF-alpha (Tumor Growth Factor-alpha), TGF-beta (Tumor Growth Factor-beta), bFGF (basic Fibroblast Growth Factor), PDGF (Platelet Derived Growth Factor) und VEGF (Vascular Endothelial Growth Factor) frei. Besonders die letzteren beiden aktivieren die Migration von Fibroblasten und Endothelzellen in das Wundbett, welches die folgende Phase der Granulation oder Proliferation einleitet.
Eine prolongierte oder überschießende Inflammationsreaktion mit dauerhaft aktivierten neutrophilen Granulozyten geht mit einer chronischen Wundheilungsstörung einher: In chronischen Wunden wurden persistierende Zytokine und freie Sauerstoffradikale nachgewiesen, welche initial zwar erforderlich sind, danach aber zurückgehen müssen, damit die nächste Phase initiiert werden kann und es sonst zur Schädigung des Gewebes kommen kann. Auch eine spätere übermäßige Narbenbildung kann hierdurch getriggert werden.
In der nachfolgenden Proliferations- oder Granulationsphase, welche sich in der Regel vom vierten bis zum siebten Tag erstreckt, bestehen weiter erhöhte Zytokin-Level vornehmlich mit Epidermal Growth Factor (EGF), Vascular Endothelial Growth Factor (VEGF) und Transforming Growth Factor beta (TGF-beta) mit begleitender erhöhter Zellaktivität. Die Erneuerung der Dermis wird durch einwandernde Fibroblasten und Endothelzellen angeregt, die Granulationsgewebe – reich an Fibrin und Fibronectin – bilden, welches wiederum Grundlage für einwandernde Keratinozyten und epitheliale Stammzellen ist. Durch die Anregung der Neoangiogenese können Sauerstoff und Nährstoffe vermehrt in das Wundbett transportiert werden. Eine zentrale Rolle in dieser Phase spielen die Fibroblasten, welche eine Extrazellulär-Matrix aus Kollagenen, Fibronectin, Glycosaminoglycanen, Proteoglycanen und Hyaluronsäure bilden, welche dann mit den Zellen interagiert und Zellmigration, Zellwachstum sowie Zelldifferenzierung induziert.
Bei Mangeldurchblutung oder Stoffwechselstörungen wird die Granulationsphase gestört. Ebenfalls können Probleme auftreten, wenn die Ausreifung der kollagenen Fasern, welche normalerweise zwischen dem sechsten und zehnten Tag beginnt, gestört ist. Hierbei kommt es zu einer Umwandlung von Kollagen Typ III in Kollagen Typ I.
Die Granulationsphase geht in die Regenerations- oder Reparationsphase ab dem achten Tag über, bei welcher die Re-Epithelisierung das offene Granulationsgewebe verschließt und damit zu einem Wundverschluss führt. Hier spielen aktivierte Keratinozyten eine wesentliche Rolle, wobei die Wundfläche etwa zu zwei Drittel durch sich teilende Keratinozyten und epitheliale Stammzellen verschlossen wird. Ein weiteres Drittel der Wundfläche wird durch die neuaufgebaute extrazelluläre Matrix mit ihren kollagenen Fasern und Fibroblasten durch Schrumpfung verkleinert. Das Ergebnis dieses ganzen Prozesses ist die Narbe, welche sich in den folgenden Monaten bis hin zu zwei Jahren noch weiter remodelliert und ausreift. Da in dem Narbengewebe keine elastischen Fasern ausgebildet werden, ist es im Vergleich weniger belastbar und reißfest. Des Weiteren enthält die Narbe keine Schweißdrüsen, Haarbälge und auch keine Melanozyten und somit keine Pigmente. Durch die Remodellierung und Vernetzung der kollagenen Fasern kann sich das Narbengewebe in gewissem Maße auf den mechanischen Umgebungsstress ausrichten. Während des Ausreifungsprozesses bildet sich das gefäßreiche Bindegewebe um und der Wasseranteil im Gewebe nimmt ab, die Narbe blasst ab und schrumpft.
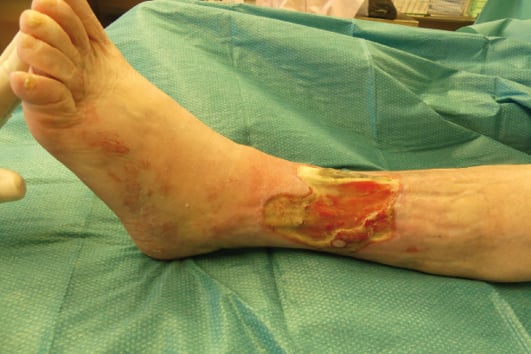
Abb. 1a: Ulcus cruris venosum
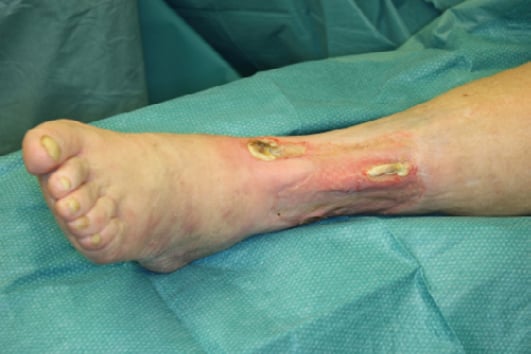
Abb. 1b: Ulcus cruris venosum drei Monate nach zunächst erfolgreicher chirurgischer Therapie (eingeheiltes Spalthauttransplantat) mit nun erneuten entzündlichen Ulcerationen und Sehnensequestern
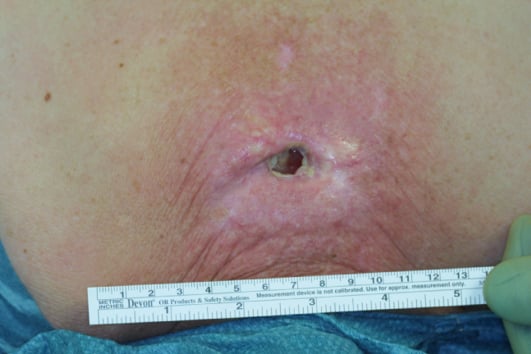
Abb. 2a: Strahlenulcus mit umgebendem Radioderm nach vormaliger Radiatio bei Syringomyelie
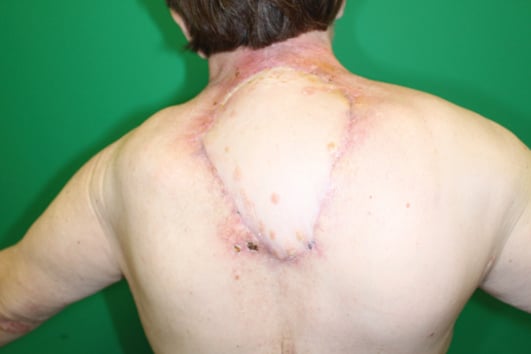
Abb. 2b: Radikale Excision unter Mitnahme des Radioderms und histologische Untersuchung, Defektdeckung mit gestielter M. latissimus dorsi Lappenplastik.
Ursachen chronischer Wundheilungsstörungen und Therapiekonzepte
Wenn der Ablauf der Wundheilung durch innere oder äußere Faktoren gestört wird, kommt es zu chronischen Wundheilungsstörungen. Als wesentliche Ursachen sind hier zum einen Durchblutungsstörungen jeglicher Art, sei es die periphere arterielle Verschlusskrankheit, die diabetische Mikroangiopathie oder die chronisch venöse Insuffizienz zu nennen. Auch akute oder chronische Druckerhöhungen im Gewebe, beispielsweise durch Lymphödeme oder kardial bedingte periphere Ödeme, wirken sich negativ auf die Wundheilungsphasen aus, ebenso wie erhöhter Druck von außen.
Einen weiteren wichtigen Störfaktor stellen Infektionen dar, welche auch durch im Körper verbliebene Fremdkörper aufrechterhalten werden können. Auch Parasitosen können die Entstehung und Aufrechterhaltung eines chronischen Wundmileus mitbedingen.
Periphere Nervenschädigungen, beispielsweise eine Polyneuropathie, prädisponieren nicht nur zu Bagatellverletzungen aufgrund fehlender Schutzmechanismen, sie beeinflussen auch Durchblutung und Wundheilung.
Mitunter verbirgt sich in einer chronischen, nicht heilenden Wunde ein Tumor. In bestrahltem Gewebe kann es auch nach Jahrzehnten zur Entstehung von Radiodermen und Strahlenulcera kommen.
Als weitere Ursachen können Störungen des Immunsystems chronische Wundheilungsstörung bedingen und aufrechterhalten, zum Beispiel durch eine immunsuppressive Therapie oder durch Autoimmunerkrankungen wie Sklerodermie, Vasculitis, mit Rheumatoider Arthriitis oder Systemischem Lupus erythomatodes assoziierte Ulcera, oder Pyoderma gangränosum. Thrombotische vaskuläre Erkrankungen wie beispielsweise die Thrombangitis obliterans (Winiwarter-Bürger), Calcyphylaxie, Kryoglobulinämie oder das Antiphospholipid-Syndrom können ebenfalls komplizierte Wunden verursachen. Weitere Faktoren sind Mangelernährung mit Protein- und Albuminmangel, Mangel wichtiger Hormone, Vitamine, Mineralien und Spurenelemente oder eine katabole Stoffwechsellage.
Meilensteine der Wundbehandlung sind zum einen die feuchte Wundbehandlung zur Förderung der Inflammations-, Granulations- und Regenerationsphase, des Weiteren die Therapie einer überschießenden inflammatorischen Situation sowie eine Infektbekämpfung durch ein radikales Debridement und Beseitigung der auslösenden Infektursache (beispielsweise eines infizierten Fremdkörpers, einer Osteomyelitis o. ä.) sowie bei systemischer Inflammationsreaktion der Einsatz einer gezielten Antibiose. Zum Einsatz kommen hier topische Antiinfektiva, enzymatische Produkte, Wundspüllösungen, antiseptische Wundauflagen, die Vakuum- oder negative Druck-Wundtherapie, der Einsatz von biologischen Helfern wie Maden oder eine topische Therapie mit Bacteriophagen.
Ein weiterer wichtiger Schritt ist die Verbesserung der lokalen Durchblutungssituation durch angiologische, radiologisch-interventionelle oder gefäßchirurgische Maßnahmen. Bei peripheren Ödemen sind Entstauungstherapie, Lymphdrainagen sowie Kompressionstherapie (sofern kardiovaskulär kompensiert) indiziert. CO2-Bäder können reinigend und durchblutungsfördernd die Wundheilung unterstützen. In speziellen Indikationen kann auch die hyperbare Sauerstofftherapie eingesetzt werden. Lampen mit wassergefiltertem Infrarot werden ebenfalls zur topischen Verbesserung der Wundheilung eingesetzt. Dermale Hautersatzprodukte können ebenfalls eingesetzt werden, um die Granulations-und Regenerationsphase zu unterstützen. Bei speziellen chronischen Wunden, beispielsweise Radiodermen, können auch lokal Fettstammzellen injiziert werden, um eine Anregung der Wundheilung durch parakrine Wachstumsfaktoren und Hormone zu erreichen. Bei durch Autoimmunerkrankungen verursachten Ulzerationen sollte der Einsatz von Immunmodulatoren erwogen werden.
Resumé
Zusammenfassend benötigt ein erfolgreiches Wundmanagement chronischer Wunden einen multimodalen Zugang, wobei auch medizinische Begleiterkrankungen beachtet und behandelt werden müssen. Die Evidenz-Lage erlaubt derzeit zwar nicht die Hervorhebung spezifischer Wundmaterialien, jedoch besteht eine Level-1 Evidenz für die zentrale Bedeutung des Débridements sowie die Aufrechterhaltung eines feuchten Wundmilieus zur Verbesserung der Wundheilung.
Literatur
[1] Groppa E et al: Immune Cell Therapies to improve regeneration and revascularization of non-healing wounds. Int J Mol Sci 2020; 21:5235
[2] Janis JE et al: Wound healing: Part I. Basic science. PRS 2016; 138:9S
[3] Jones RE et al: Management of chronic wounds – 2018; JAMA 2018; 320(14): 1481-1482
[4] Shanmugarm VK et al: Vasculitis and autoimmune wounds. J Vasc Surg Venous Lymph Disord 2017;5(2):280-292
[5] Sorg H et al: Skin Wound Healing: An update on current knowledge and concepts. Eur Surg Res 2017; 58:81-94
[6] Zhao R et al: Inflammation in chronic wounds. Int J Mol Sci 2016; 17:2085
Weyand B, Vogt PM: Wenn Wunden nicht heilen – Pathophysiologie und Therapiemöglichkeiten chronischer Wunden. Passion Chirurgie. 2021 Januar/Februar; 11(01/02): Artikel 03_01.
















