Kutane Malignome stellen die häufigsten bösartigen Erkrankungen überhaupt dar und zeigen eine seit Jahrzehnten ansteigende Inzidenz. Das Basalzellkarzinom (BZK), das kutane Plattenepithelkarzinom (PEK) sowie das maligne Melanom (MM) sind hierbei die führenden Entitäten. Allen Entitäten gemeinsam ist ätiologisch eine erhöhte UV-Exposition. Das Risiko steigt mit zunehmender UV-Exposition und damit mit dem Alter, wobei als weitere Kofaktoren unter anderem ein heller Hauttyp, Immunkompromittierung, chronische Entzündungen, Noxen und ionisierende Strahlung sowie HPV-Infektion und Genodermatosen hinzukommen können. Über 75% aller BZKs und PEKs sind dabei in der Kopf-Hals-Region und hier vorwiegend im Bereich der Gesichtshaut lokalisiert. Grundsätzlich sollten malignomsuspekte Hautveränderungen histologisch mittels Biopsie oder Probeexzision bzw. Exzisionsbiopsie abgeklärt werden. Ihre Therapie muss somit neben stadienspezifischen Konzepten insbesondere die anatomischen, funktionellen und ästhetischen Aspekte der Kopf-Hals-Region berücksichtigen.
Basalzellkarzinom des Kopf-Hals-Bereiches
Das Basalzellkarzinom (BZK) ist der häufigste bösartige Tumor des Menschen überhaupt (jährliche Inzidenz über 200 Neuerkrankungen pro 100.000 in Deutschland) und stellt ca. 80% der nicht-melanozytären Hauttumore dar. Die häufigste Lokalisation findet sich im besonders UV-exponierten Kopf-Hals-Bereich, insbesondere dem Gesicht. Zwar ist eine Metastasierung extrem selten und auf Einzelfälle sowie aggressivere Subtypen und Mischformen (metatypisches BZK, basosquamöse Karzinome) beschränkt, jedoch wachsen BZK lokal destruierend. Von den verschiedenen Subtypen spielen insbesondere das eher gut abgegrenzte noduläre BZK sowie die deutlich schwieriger hinsichtlich der Tumorgrenzen beurteilbaren sklerodermiformen und ulcerösen („Basalioma terebrans“) klinisch die größte Rolle (Abb. 1). Rezidivrisiko und Komplexität der Therapie steigen mit zunehmender Größe und insbesondere steigender Tumordicke sowie Invasionstiefe. Bei Erreichen tieferliegender Strukturen wie Muskeln oder Knochen sollte eine Schnittbildgebung (CT, MRT) erfolgen. [1, 2]
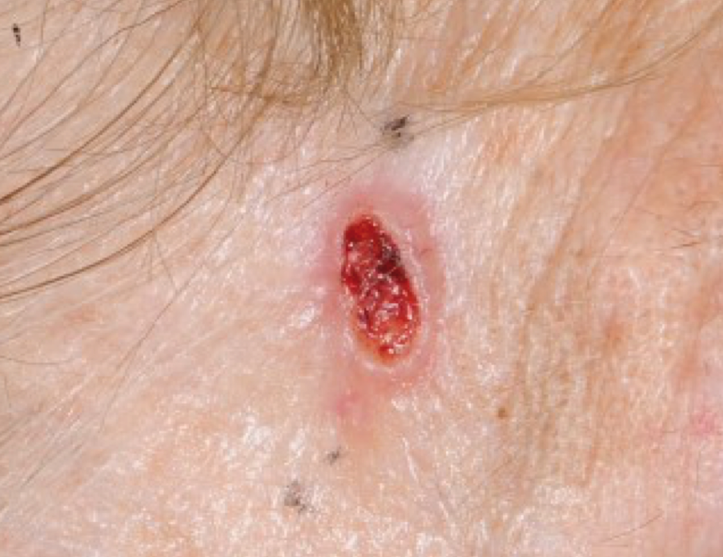
Abb. 1: Basalzellkarzinom (BZK oder BCC) der Schläfe.
Nur für sehr oberflächliche oder multizentrische BZK sowie bei stark reduziertem Allgemeinzustand / Inoperabilität sollten lokal-topische Oberflächentherapien (Kryotherapie, Imiquimod, 5-Floururacil-Salbe, Laserablation etc.) als Alternative zu einer operativen Therapie oder Strahlentherapie erwogen werden.
In erster Linie stellt die operative Resektion eines BZK das Verfahren der Wahl dar. Hierbei gilt der Erzielung tumorfreier Resektionsränder (R0) besondere Aufmerksamkeit, um das Rezidivrisiko zu senken. Im Gesichtsbereich ist hier eine randschnittkontrollierte Aufarbeitung des Exzidates (histographische / mikrographische Chirurgie) einzufordern, um möglichst schonend vorzugehen und gesundes Gewebe soweit möglich zu erhalten [3]. Bei größeren Defekten, die eine Lappenplastik erforderlich machen, sollte ein zweizeitiges Verfahren (Defektdeckung mittels meist lokoregionärer Lappenplastik erst in einer zweiten OP nach Erreichen einer histologisch gesicherten R0-Resektion) favorisiert werden.
Die operative Therapie im Gesichtsbereich erfordert profunde Kenntnisse der Anatomie sowie Funktion und muss auch ästhetische Aspekte mitberücksichtigen. Abbildung 2 zeigt exemplarisch das klinische Beispiel einer aufwändigen Lidrekonstruktion nach Resektion eines BZK der Unterlidkante. Im Gesichtsbereich dominieren dabei lokale und regionäre Lappenplastiken. In fortgeschrittenen Fällen kommen auch freie oder gestielte Fernlappenplastiken zum Einsatz, bei Verlust ganzer Gesichtsorgane (Ohr, Nase, Auge) auch die Rehabilitation mittels Gesichtsepithesen.
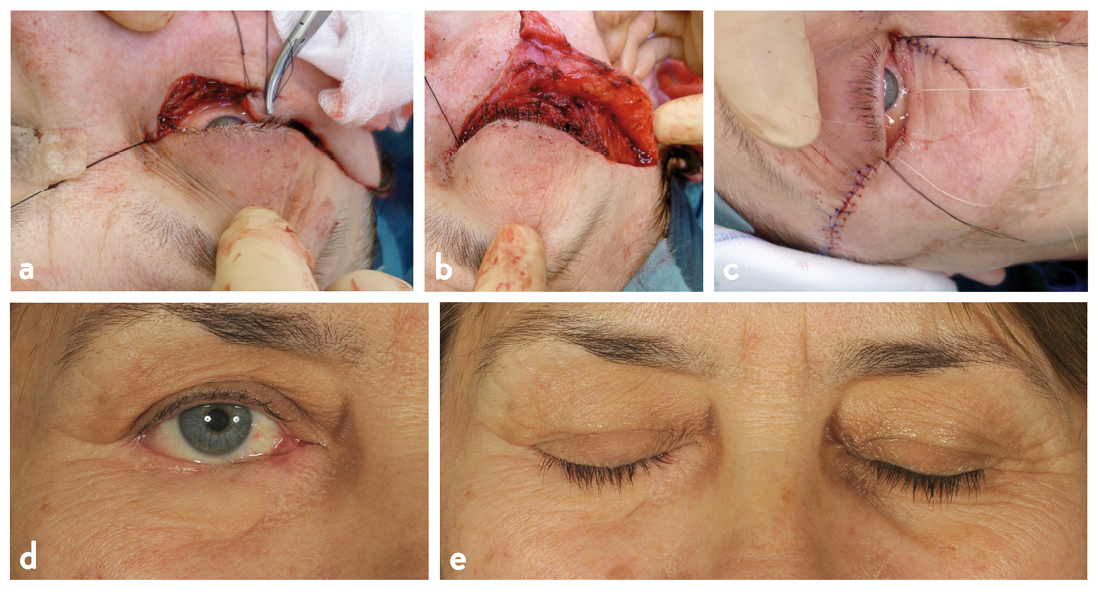
Abb. 2: Rekonstruktion eines 2/3-Defektes des rechten Unterlides nach Basaliomresektion mittels extendierter Tenzelplastik:Defekt (a), Lappenhebung (b), Wundverschluss (c), Resultat mit suffizientem Lidschluss 1 Jahr post-OP ohne weiteren Korrektureingriffe (d, e).
Alternativ zur Operation stellt auch die Strahlentherapie eine gute Option zur Behandlung des BZK dar. Des Weiteren steht für lokal weit fortgeschrittene BZK, bei lokaler oder allgemeiner Inoperabilität, bei Ablehnung eines operativen Vorgehens oder im seltenen Fall einer Metastasierung als Systemtherapie medikamentös die Therapie mit einem Hedgehog-Inhibitor (Erivedge®) oder ggf. auch PD-L1-Inhibitor zur Verfügung.
Kutanes Plattenepithelkarzinom der Kopf-Hals-Region
Mit einer Inzidenz von 80–100 pro 100.000 Einwohnern und damit geschätzt fast 50.000 jährlichen Neuerkrankungen stellt das Haut-PEK 20% aller nicht-melanozytären Hauttumore dar (Abb. 3). Vorstufen invasiver Karzinome sind häufig aktinische Keratosen, im Bereich des Lippenrotes die aktinische Cheilitis, das Carcinoma in situ und der M. Bowen. Somit kommt auch hier der Prävention und dem Hautkrebsscreening zur Erkennung von Vorläuferläsionen und Frühstadien eine besondere Rolle zu. Insgesamt erkranken Männer ca. doppelt so häufig wie Frauen [4, 5].
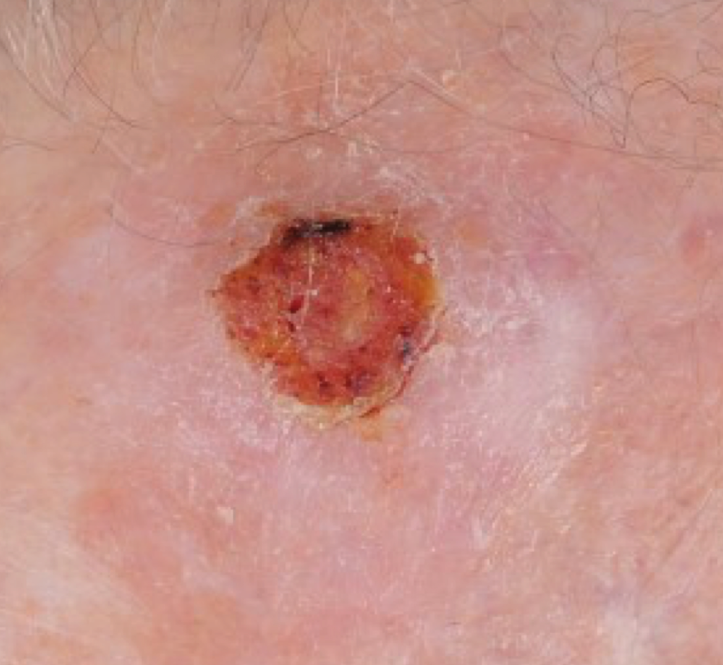
Abb. 3: Plattenepithelkarzinom (PEK) der Stirn.
Das kutane Plattenepithelkarzinom kann in ca. 5% der Patienten lymphogen metastasieren. Infobox 1 stellt Risikofaktoren und Lokalisationen mit deutlich erhöhtem Metastasierungsrisiko zusammen (High-risk-PEK). Mit Metastasierungsraten von 6–8 % bzw. bis zu 10% stellen im Gesichtsbereich insbesondere Lippe und Ohr Risikoregionen dar. Die Stadieneinteilung erfolgt anhand der TNM-Klassifikation gemäß AJCC (Tabelle 1) [6]. Die Stadieneinteilung korreliert mit der Prognose. Im Rahmen des Stagings sind neben klinischer Untersuchung des gesamten Integuments (Screening auf Zweitmalignome) und einer Sonographie der ableitenden Lymphwege ab dem Stadium III auch schnittbildgebende Verfahren (CT, MRT) sinnvoll.
|
Infobox 1: Prognostische Faktoren für ein erhöhtes Metastasierungrisiko und schlechteres krankheits-spezifischen Überleben beim kutanen PEK [6].
|
Tab. 1: TNM-Klassifikation des kutanen PEK (AJCC / UICC (8. Auflage, 2017))
|
T-Kategorie |
|
|
TX |
Primärtumor kann nicht beurteilt werden |
|
T0 |
Kein Anhalt für Primärtumor |
|
Tis |
Carcinoma in situ |
|
T1 |
Tumor 2 cm oder weniger in größter Ausdehnung |
|
T2 |
Tumor mehr als 2 cm, aber nicht mehr als 4 cm in größter Ausdehnung |
|
T3 |
Tumor mehr als 4 cm in größter Ausdehnung oder oberflächliche Knocheninvasion oder perineurale Invasion oder tiefe Invasion* |
|
T4a |
Tumor mit makroskopischer Knocheninvasion/ Knochenmarksinvasion |
|
T4b |
Tumor mit Invasion des Achsenskeletts eingeschlossen Foramina und/oder Beteiligung des vertebralen Foramens bis zum Epiduralraum |
|
* „tiefe Invasion“ ist definiert als Invasion jenseits des subkutanen Fettgewebes oder >6 mm (gemessen vom Stratum granulosum der benachbarten Epidermis bis zur Basis des Tumors) Eine perineurale Invasion als Kriterium für T3 ist definiert als klinische oder radiologische Beteiligung benannter Nerven ohne Beteiligung der Foramina oder der Schädelbasis. |
|
|
N-Kategorie |
|
|
N0 |
Keine regionären Lymphknotenmetastasen |
|
N1 |
Metastase(n) in einem regionären Lymphknoten, 3 cm oder weniger in größter Ausdehnung |
|
N2 |
Metastase(n) wie nachfolgend beschrieben: |
|
N2a |
Metastase(n) in solitärem ipsilateralen Lymphknoten, mehr als 3 cm, aber nicht mehr als 6 cm in größter Ausdehnung, ohne extranodale Ausbreitung |
|
N2b |
Metastasen in multiplen ipsilateralen Lymphknoten, keiner mehr als 6 cm in größter Ausdehnung, ohne extranodale Ausbreitung |
|
N2c |
Metastasen in bilateralen oder kontralateralen Lymphknoten, keiner mehr als 6 cm in größter Ausdehnung, ohne extranodale Ausbreitung |
|
N3a |
Metastase(n) in einem Lymphknoten, mehr als 6 cm in größter Ausdehnung, ohne extranodale Ausbreitung |
|
N3b |
Metastase(n) in einem einzelnen oder multiplen Lymphknoten, klinisch in extranodaler Ausbreitung* |
|
* Das Vorhandensein einer Beteiligung (Invasion) der Haut oder der Weichteile oder klinische Zeichen einer Nervenbeteiligung wird als klinische extranodale Ausbreitung angesehen. |
|
|
M-Kategorie |
|
|
M0 |
Keine Fernmetastasen |
|
M1 |
Fernmetastasen |
Therapie der ersten Wahl ist bei allen resektablen Tumoren mit kurativer Intention die komplette chirurgische Entfernung (R0-Resektion). Der übliche klinische Sicherheitsabstand sollte mindestens 5 mm betragen, wobei im Gesichtsbereich bei kritischen Lokalisationen (z. B. am Unterlid) auch eine Unterschreitung möglich ist. Wie schon bei der Chirurgie des BZK, sollte im Gesichtsbereich wenn möglich grundsätzlich eine randschnittkontrollierte histographische Aufarbeitung (mikrographische Aufarbeitung) erfolgen. Eine definitive Defektdeckung mit lokalen, regionalen oder auch freien bzw. gestielten Fernlappenplastiken sollte nur bei gesicherten tumorfreien Resektionsrändern erfolgen. Damit ist in vielen Fällen ein zweizeitiges Vorgehen, also die Defektrekonstruktion in einer sekundären OP nach Erreichen der histologisch gesicherten R0-Resektion, zu favorisieren. Je nach klinischem und histologischem individuellem Befund kann – z. B. bei angestrebter plastischer Sofortrekonstruktion, wie im Bereich der Lippen und Lider indiziert – auch eine intraoperative Schnellschnittkontrolle hilfreich sein.
Bei High-Risk-PEKs (siehe Infobox 1) kann zusätzlich eine Lymphknotenchirurgie mittels Wächterlymphknoten-Biopsie (SLNB), ggf. auch eine elektive Lymphknoten-Ausräumung (z. B. als selektiv-funktionelle Neck Dissection relevanter Level) erwogen werden. Je nach Risikostratifizierung ist dieses z. B. beim PEK der Lippe und des Ohres sinnvoll [7–9]. Bei klinisch oder bildgebend gesicherten Metastasen sollte auf jeden Fall eine Lymphknotendissection (therapeutische Neck Dissection und / oder Parotidektomie) erfolgen.
Eine Strahlentherapie kann adjuvant erfolgen bei nodaler Metastasierung oder Risikobefunden wie perineuralem Wachstum, Lymphgefäßinvasion und inkompletter Entfernung (R1/R2-Status). Bei Inoperabilität (lokal oder allgemein, z. B. bei stark reduziertem Allgemeinzustand) bietet eine Radiatio, ggf. in Kombination mit einer medikamentösen Systemtherapie, eine potentiell auch kurative Option.
Fernmetastasierte Patienten sollten nach Tumorboard-Entscheidung einer onkologischen medikamentösen Systemtherapie zugeführt werden. Neben den bisherigen Chemotherapeutika steht hier seit kurzem auch ein zugelassener PD-1-Inhibitor (Cemiplimab) zur Verfügung [6].
Tabelle 2 gibt einen zusammenfassenden Überblick über stadienadaptierte Therapieoptionen.
Tab. 2: Stadienadaptierte Therapieoptionen beim kutanen Plattenepithelkarzinom der Kopf-Hals-Region
|
Stadium |
1. Wahl |
weitere Optionen |
|
|
I |
T1, N0 |
OP, ggf. SLNB |
prim. RT |
|
II |
T2, N0 |
OP, ggf. SLNB |
prim. RT |
|
III |
T3, N0 |
OP, ggf. SLNB / LAD |
prim. RT |
|
III |
T1–3, N1 |
OP inkl. LAD, |
prim. RT / RCT |
|
IV |
T4, jedes N |
OP inkl. LAD, adj. RT/ RCT |
prim. RT / RCT |
|
IV |
jedes T, N2–3 |
OP inkl. LAD, prim. RT / RCT |
palliative Systemth. |
|
IV |
jedes T, jedes N, M1 |
palliative Systemth. palliative RT / RCT |
Metastasektomie / palliative OP |
|
Legende: OP = operative Tumorresektion und Defektdeckung / Rekonstruktion RT = Radiatio RCT = kombiniert Radio-Chemo-Therapie SLNB = Wächterlymphknotenbiopsie bei High-risk-PEK LAD = Lymphadenektomie (Neck dissection, Parotidektomie) Systemth. = systemische palliative Therapie (Chemotherapie, Immuntherapie) adj. = adjuvant prim. = primäre |
|||
Merkelzellkarzinom
Das Merkelzellkarzinom (MCC) ist ein bösartiger primärer Tumor der Haut. Mit einer Inzidenz von 0,1 – 0,2/100.000 ist er deutlich seltener als das Basalzellkarzinom, das Plattenepithelkarzinom oder das maligne Melanom [10]. Es zeigen sich, wie bei den anderen Entitäten, deutliche regionale Unterschiede sowie ein deutlicher Anstieg in der Häufigkeit in den letzten Dekaden [11]. In mehr als der Hälfte der Fälle ist die Kopf-Hals-Region betroffen, gefolgt von den oberen und unteren Extremitäten [12]. Daher wird ätiologisch, wie auch bei den anderen Entitäten, ein Einfluss der UV-Exposition diskutiert, wobei neue Publikationen auch eine virale Genese postulieren [13]. Gleichzeitig ist die Inzidenz bei Patienten mit Immunsuppression, insbesondere nach Organtransplantation, hämatologischen Erkrankungen und bei HIV-Infektionen deutlich erhöht. Betroffen sind maßgeblich Patienten, die älter als 65 Jahre sind, wobei Männer gegenüber Frauen doppelt so häufig erkranken [14].
Klinisch imponiert das MCC typischer Weise als solider violetter Knoten mit glänzender Oberfläche von weicher Konsistenz (Abb. 3), wobei aber insbesondere im Bereich des Stamms auch flache plaqueartige Läsionen beschrieben werden [15]. Das Erscheinen kann zunächst unspezifisch sein und die Diagnose ist daher nicht selten deutlich verzögert. Beweisend ist die histologische bzw. immunhistochemische Aufarbeitung.
Die Prognose des MCC ist streng mit dem Stadium der Erkrankung assoziiert. Ausschlaggebend ist hier maßgeblich die Größe des Primärtumors: Die 5-Jahresüberlebensrate sinkt von Stadium I (<2 cm) mit 75 % auf 50 % im Stadium II (>2 cm). Während bei regionären Lymphknotenmetastasen (Stadium III) ebenfalls eine 5-JÜ von um die 50 % beschrieben werden, sinkt diese bei manifesten Fernmetastasen im Stadium IV auf unter 20 %. [16–19] Einen zusätzlichen Einfluss auf die Prognose hat die hohe Rezidivrate, die lokal bei ca. 10 % und regionär/distant bei um die 20 % zu liegen scheint [20, 21].
Diagnostisch sollte bei dem Verdacht auf ein MCC eine sofortige bioptische Sicherung oder bei kleineren Befunden eine vollständige Exzision erfolgen, da Biopsien aufgrund der vermeintlichen Verschlechterung der Prognose gegenüber der einzeitigen Resektion mit Sicherheitsabstand immer wieder in Frage gestellt werden. Bei Bestätigung wird im Rahmen des Stagings die Sonographie bzw. Schnittbildgebung der regionären Lymhabflusswege sowie ein Ganzkörperstaging mittels 18F-FDG-PET/CT oder alternativ mittels CT von Thorax/Abdomen und einer MRT des Schädels empfohlen. [22] Gleichzeitig wird auch bei klinischer N0-Situation (cN0) die Sentinel Lymph-Node Biopsie (SLNB) dringend angeraten.
Therapeutisch steht die chirurgische Resektion im Gesunden im Vordergrund. Hier sollten, abhängig von der Tumorgröße als klinischer Sicherheitsabstand im Stadium I ein cm und im Stadium II zwei cm angestrebt werden. Auch wenn im Kopf-Hals-Bereich aufgrund der Prämisse der Vermeidung mutilierender Eingriffe geringere Sicherheitsabstände akzeptiert werden, wird von dem sonst häufig bei kutanen Malignomen befürworteten Verfahren der Moh’s Surgery aufgrund der hohen Rate von in transit Metastasen abgeraten.
Ob sich bei einer in der SLNB detektierten N+-Situation allerdings eine komplettierende Lymphadenektomie anschließen sollte, ist bisher nicht eindeutig beantwortet, da bislang ein Einfluss auf das Gesamtüberleben nicht gezeigt werden konnte. Dies muss daher mit dem Betroffenen individuell besprochen werden [23, 24]. Bei manifesten Metastasen (cN+) sollte aber eine Lymphadenektomie in das primäre Therapiekonzept integriert werden.
Beim MCC handelt es sich um einen prinzipiell strahlensensiblen Tumor, so dass ggf. auch eine primäre Strahlentherapie (RT) diskutiert werden kann. Eine klare Indikation zur adjuvanten RT ergibt sich im Stadium II und bei nicht ausreichenden Resektionsgrenzen. Der Nutzen der adjuvanten RT im Stadium I nach Resektion mit adäquatem Sicherheitsabstand ist nicht abschließend geklärt. Um eine zeitnahe Einleitung der Strahlentherapie zu ermöglichen, sollte beim chirurgischen Vorgehen eine entsprechende, zeitnahe Defektrekonstruktion von vornherein in die Planung mit einbezogen werden.
Gleichzeitig scheint es bei einer N+-Situation (im Rahmen der SLNB detektiert oder nach Lymphadenektomie) einen Vorteil der adjuvanten RT in Hinsicht auf die lokoregionäre Kontrolle zu geben.
Der Einsatz der systemischen Therapie ist bei lokal nicht beherrschbarer Erkrankung oder distanten Metastasen indiziert, wobei durch Zytostatika zwar gute Remissionsraten von bis zu 60 % aber nur ein kurzes progressionsfreies Intervall von 8 Monaten erreicht werden können [25, 26]. Zukünftig könnte hier durch den Einsatz der Immuntherapie eine Verbesserung erzielt werden, insbesondere der Einsatz der zielgerichteten Therapie (PD1 und PD-L1) ist aktuell in Erforschung.
Malignes Melanom
Das kutane Maligne Melanom (cMM) ist wohl der am extensivsten untersuchte Tumor der Haut, der sich insbesondere durch seine hohe Metastasierungsrate auszeichnet. Mit einer Inzidenz von ca. 25/100.000 in Deutschland ist er deutlich seltener als das Basalzellkarzinom oder das Plattenepithelkarzinom, aber dennoch für 90 % der Todesfälle aller Hauttumore verantwortlich [27]. Man unterscheidet verschiedene Subtypen (Abb. 4, 5, 6) mit unterschiedlicher Häufigkeit und Prognose [28].
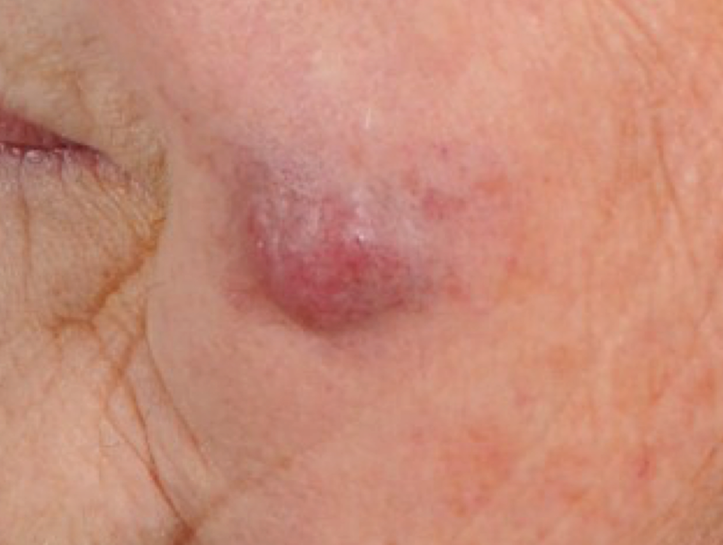
Abb. 4: Merkelzellkarzinom (MCC) im Bereich der linken Wange
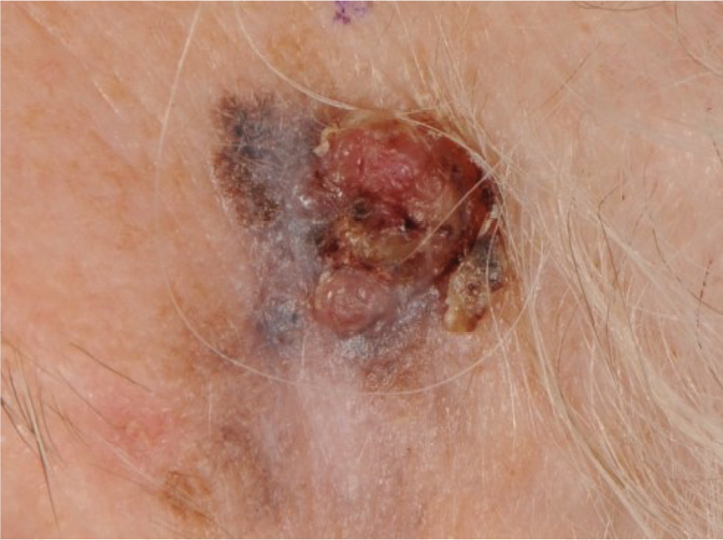
Abb. 5: Noduläres MM der linken Schläfe
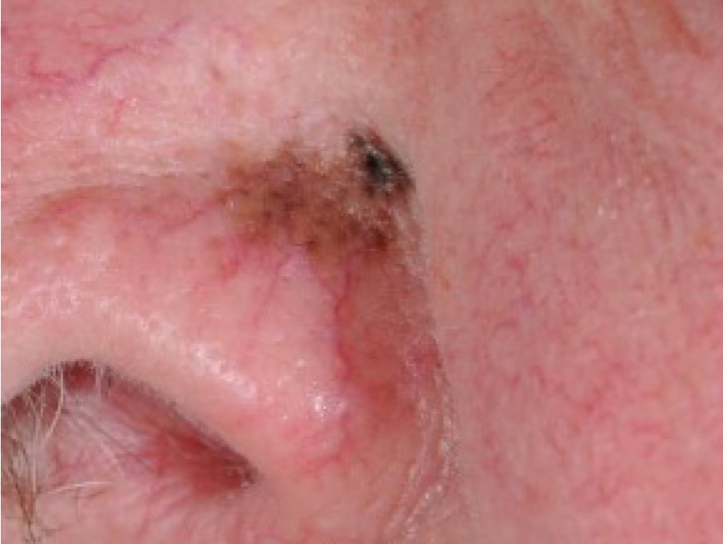
Abb. 6: Lentigo Maligna Melanom des Nasenflügels li
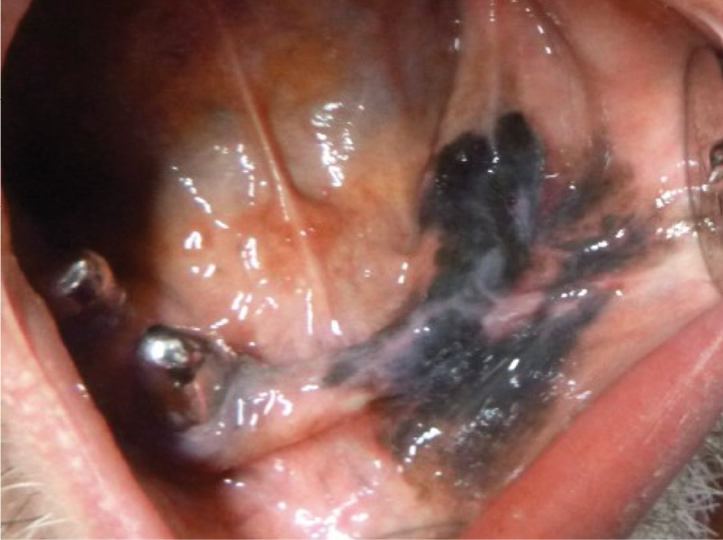
Abb. 7: Mukosales malignes Melanom des linken Mundboden pT3
Das superfiziell spreitende Melanom stellt mit 60 % den häufigsten Typ dar und tritt häufig am Stamm und den Extremitäten auf. 20 % der Melanome sind vom nodulären, das heißt knotigen Typ. Die braunen bis blauschwarzen, mitunter auch roten Knoten sind glatt, können aber frühzeitig ulzerieren und bluten dann leicht. Auch noduläre Melanome betreffen vorwiegend den Rücken, die Brust, Arme und Beine. Lentigo maligna Melanome wachsen bevorzugt an lichtexponierten Stellen der Kopf-Hals-Region. Ihr Erscheinen ist häufig unspezifisch und kann hell- bis dunkelbraun oder weiß- bis blaugrau sein. Das akral lentiginöse Melanom ist der seltenste Melanom-Typ und betrifft die Finger und Zehen, aber auch Handflächen, Fußsohlen und das Nagelbett. Hiervon abzugrenzen ist die mukosale Variante des Melanoms, das nur ca. 1–3 % der malignen Melanome ausmacht.
Wie bei den anderen Entitäten der Hauttumore zeigen sich deutliche regionale Unterschiede sowie ein dramatischer Anstieg in der Häufigkeit in den letzten Dekaden. [28] Ätiologisch gilt eine starke, wiederkehrende UV-Belastung mit Sonnenbränden vor allem im Kindes- und Jugendalter als wichtigster Risikofaktor. [29] Weitere Risikofaktoren sind das atypische Nävussyndrom, eine positive Familienanamnese, ein malignes Melanom in der eigenen Vorgeschichte sowie eine Immunsuppression. [30]
Beide Geschlechter sind etwa gleich häufig betroffen, wobei das durchschnittliche Erkrankungsalter bei Frauen mit 60 Jahren unter dem von Männern (68 Jahre) liegt.
Die Prognose ist, neben der Einstufung der Ulzeration, maßgeblich mit der Tumordicke assoziiert. Die 5-Jahresüberlebensrate sinkt bereits von Stadium Ia (TD <1 mm) zu Stadium Ib (TD>1 mm).
Diagnostisch sollte bei dem Verdacht auf ein MM eine sofortige vollständige Exzision erfolgen. Da zur abschließenden histologischen Diagnosesicherung die Beurteilung des gesamten Tumors erforderlich ist, wird zunächst nur die komplette Exzision mit einem Sicherheitsabstand von ungefähr 2 mm empfohlen. [31, 32]
Bei Bestätigung der Diagnose werden im Rahmen des Stagings der Stadien Ia, Ib, und IIa neben der Ganzkörperuntersuchung die Sonographie der regionären Lymphabflusswege sowie die Bestimmung des S100B-Level empfohlen. Ab Stadium IIb kann, ab dem Stadium IIc sollte zusätzlich eine Bestimmung des Serum-Laktatdehydrogenase-Spiels (LDH) und ein Ganzkörperstaging mittels CT von Thorax /Abdomen und ein MRT des Schädels durchgeführt werden. [31] Alternativ kann auch 18F-FDG-PET/CT erfolgen (Infobox 2).
Infobox 2: Modifizierter Algorithmus zur Diagnostik und Therapie bei Malignem Melanom (modifiziert nach Hogrebe in Anlehnung an: Diagnostik, Therapie und Nachsorge des Melanoms, Langversion 3.2, 2019, AWMF Registernummer: 032/024OL)
|
Td. |
in situ |
0–1 mm |
1–2 mm |
2–4 mm |
ab 4 mm |
N+ |
M+ |
|||
|
T |
Tis |
1 |
2 |
3 |
4 |
|||||
|
UICC |
0 |
I |
* |
II |
III |
IV |
||||
|
Staging |
GKU |
+ Sono Hals + S100 |
** |
+ MRT Kopf + Ganzkörper CT + LDH |
||||||
|
SA |
(0,5 cm) |
1 cm |
2 cm |
|||||||
|
SLN |
nein |
ja (< 40 J.: ab 0,75 mm) |
primäre Neck |
|||||||
|
Neck |
nein |
Metastasendurchmesser (<0,1 mm: nein) 0,1 – 1 mm: kann ab 1 mm: sollte |
||||||||
|
Onko-Konsil |
nein |
bei in-transit Metastasen |
ja |
BRAF-Status, ggf. Tuko |
Tuko |
|||||
|
RTx |
nur bei inoperablem Tumor |
> 3LK / > 3 cm / Kapseldurchbruch / lymphogenes Rezidiv |
||||||||
|
Nachsorge |
GKU |
+ Sono Hals |
** |
+ Schnittbildgebung |
||||||
|
* ab T2 mit Ulzeration ** ab T4 mit Ulzeration Laterale Parotidektomie bei Primärtumor der Wange, lateralen Stirn, Schläfe oder Kopfhaut ventral des Gehörganges Röntgen Thorax und Sono Abdomen nicht indiziert Für mukosale Melanome gelten andere Kriterien |
||||||||||
Gleichzeitig wird auch bei klinischer N0-Situation die Sentinel Lymph-Node Biopsie (SLNB) ab Stadium Ib dringend empfohlen. Bei zusätzlichen Risikofaktoren für einen positiven Wächterlymphknoten sollte die SLNB auch bei dünneren Primärtumoren (0,75–1 mm) durchgeführt werden, dazu gehören Ulzeration und/oder erhöhte Mitoserate und/oder ein jüngeres Lebensalter (<40 Jahre).
Therapeutisch steht die chirurgische Resektion im Gesunden im Vordergrund, da diese die einzige kurative Behandlung des Melanoms darstellt.
Bei Melanomen bis zu einem mm Tumordicke ist nach den vorliegenden Studiendaten ein seitlicher Sicherheitsabstand von 1 cm ausreichend [33]. Bei Melanomen über 2 mm Tumordicke sollte ein Sicherheitsabstand von 1–2 cm, wenn möglich, angestrebt werden. Weitreichendere Resektionen zeigen statistisch keinen signifikanten Vorteil im Gesamtüberleben [34, 35].
Zur Tiefe wird heute die Resektion im Gesunden als ausreichend akzeptiert. Die früher postulierte operative Entfernung der darunterliegenden Faszie hat keinen Einfluss auf die Rezidivrate oder das Überleben und kann daher auch nicht mehr empfohlen werden [36].
Bei allen Patienten mit invasivem malignem Melanom besteht das Risiko einer lymphogenen Metastasierung. Daher ist für die initiale Ausbreitungsdiagnostik die Untersuchung der Lymphknotenstationen dieser Patienten wichtig [31]. Wie oben beschrieben, sollte im Rahmen der Therapie auch bei cN0-Situation ab dem Stadium Ib und bei weiteren Risikofaktoren eine SLNB durchgeführt werden.
Zeigt sich im Rahmen der SLNB-Diagnostik eine N+-Situation, muss abhängig von der Metastasenausdehnung vorgegangen werden. Allerdings ist nicht abschließend geklärt ob eine komplettierende Lymphadenektomie Einfluss auf das Gesamtüberleben hat.
Aktuelle Daten befürworten folgendes Vorgehen:
Bei einer einzelnen LK-Metastase (Absiedlung <0,1 mm) wird keine ergänzende LAD empfohlen. Bei einer Manifestation im LK zwischen 0,1–1 mm kann eine LAD erwogen werden. Erst ab einer Metastasengröße >1 mm oder bei Vorliegen weiterer Risikofaktoren wie dem extrakapsulären Wachstum sollte eine komplementierende LAD durchgeführt werden [37, 38]. Bei cN+ sollte aber eine Lymphadenektomie in das primäre Therapiekonzept integriert werden.
Die Ausdehnung der Lymphadenektomie ergibt sich aus der Lokalisation des Primarius und/oder der detektierten Metastasen [39, 40]. Für den Kopf-Hals-Bereich ergibt sich insbesondere die Frage der Ausräumung der Parotisloge.
Der adjuvante Therapiebereich des cMM ist fortwährenden Weiterentwicklungen der Forschung unterworfen. Hier ergeben sich täglich neue Details mit neuesten Studienergebnissen und die Überlebenswahrscheinlichkeit der Patienten hat sich in den letzten Jahren dramatisch verbessert. Neben der Strahlentherapie und der Interferontherapie sind hier insbesondere die Therapie mit Checkpoint-Inhibitoren (anti-PD1-Antikörper) und Signaltransduktionsinhibitoren (BRAF- und MEK-Inhibitor) zu nennen. Die Entscheidung sollte hier interdiszipliär gefällt werden.
Seltene Hautmalignome
Zu den eher seltenen Hauttumoren gehören das atypische Fibroxanthom, dermale und pleomorphe Sarkome sowie Angiosarkome. Auch bei diesen Entitäten stellt eine komplette chirurgische Resektion das Verfahren der Wahl dar. Insbesondere bei Angiosarkomen kann dabei das Erreichen tumorfreier Resektionsränder (R0-Resektion) schwierig sein und zu großflächigen, mutilierenden Defekten führen. Bei den aggressiveren Entitäten (pleomorphes Sarkom, kutanes Angiosarkom) ist eine adjuvante Radiatio der Primärtumorregion mit einer signifikant besseren lokoregionären Kontrolle assoziiert und somit zu empfehlen. Ebenso sollte auch das Risiko lokoregionärer Satelliten- und Lymphknoten-Metastasen chirurgisch oder strahlentherapeutisch berücksichtigt werden [41].
Raguse J-D, K. Wermker K: „The big Four“ – BCC, PEC, MM & MCC: Stadiengerechte Therapie von Hautmalignomen der Kopf-Hals-Region. Passion Chirurgie. 2021 April; 11(04): Artikel 03_03.