01.12.2021 Fachübergreifend
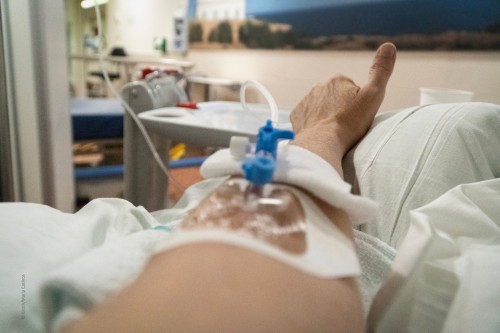
Postoperative Ernährung
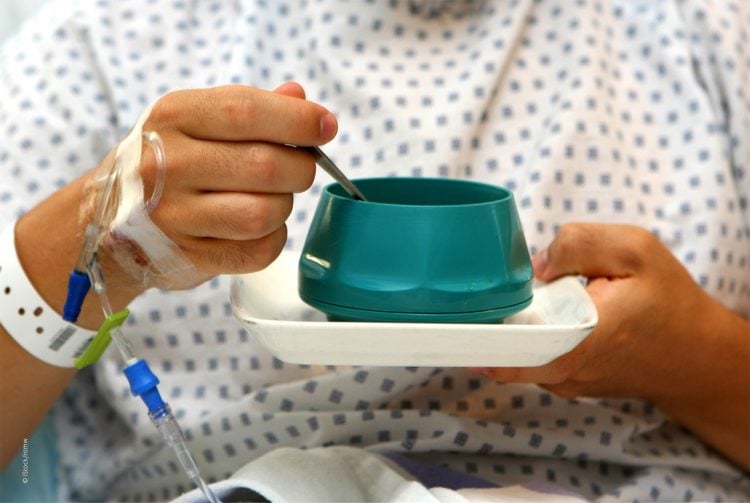
Der Standard der perioperativen Medizin ist die Behandlung in einem Enhanced Recovery after Surgery Protokoll (ERAS). Dies fordert den frühestmöglichen oralen Kostaufbau. ERAS ist vor allem auch ein metabolisches Konzept, in dem das multimodale Therapiebündel auch auf Wiederherstellung der normalen Darmmotilität und frühzeitige Toleranz einer oralen Ernährung zielt [1–3]. Eine aktuelle Metaanalyse von fünf randomisierten Studien hat gezeigt, dass auch nach abdominellen Notfalleingriffen eine frühe orale Nahrungszufuhr mit einer verminderten Letalität einhergehen kann. [4]. So erscheint im Plan A die perioperative ggf. auch künstliche Ernährungstherapie redundant. Für den Fall eines protrahierten Kostaufbaus oder sogar des Eintretens von Komplikationen mit Relaparotomie und sogar Intensivtherapie ist jedoch ein Plan B als Ernährungstherapie erforderlich [3, 5]. Diese gilt umso mehr sofern bereits präoperativ ein metabolisches Risiko diagnostiziert wurde.
Indikation zur Ernährungstherapie
Die chirurgischen Leitlinien der Europäischen Gesellschaft für Klinische Ernährung und Stoffwechsel (ESPEN) empfehlen als Indikation zur Ernährungstherapie [2]: Eine perioperative Ernährungstherapie sollte begonnen werden, wenn vorhersehbar der Patient für mehr als fünf Tage zur oralen Nahrungszufuhr unfähig sein wird. Diese ist auch indiziert, wenn mit der oralen Zufuhr voraussichtlich über mehr als 7 Tage nicht mehr als 50 % der empfohlenen Energiemenge erreicht werden.
Die folgende Übersicht stellt anhand der Leitlinie Chirurgie der Europäischen Gesellschaft für Klinische Ernährung und Stoffwechsel (ESPEN) und aktueller in zwei eigenen Übersichten zusammengefassten Daten die postoperative Ernährungstherapie dar [2, 5, 6].
Essenziell ist auch im ERAS die präoperative Erkennung von Risikopatienten z. B. mit dem gut validierten Nutritional Risk Score der ESPEN nach Kondrup [7, 8].
Früher oraler Kostaufbau – der Plan A
Im Allgemeinen und auch nach Operationen am unteren Gastrointestinaltrakt kann der orale Kostaufbau innerhalb von Stunden begonnen werden (ESPEN A Empfehlung) [2]. Die orale Nahrungszufuhr sollte sich vor allem nach der individuellen Toleranz und der Art der durchgeführten Operation richten. Ältere Patienten bedürfen besonderer Aufmerksamkeit [2].
Hier können auch Trinknahrungen, in kleinen Portionen über den Tag verteilt, zum Einsatz kommen.
Empfehlungen:
- sehr fettarm (max. 30 g Fett / Tag)
- Einsatz von leicht verdaulichen, mageren Eiweißträgern
- kohlenhydratbetont
- ballaststoffreduziert
In einer prospektiven Studie von 50 Patienten mit großer abdominaler Operation waren in den ersten sieben Tagen postoperative Energie- und Eiweißaufnahme bei der Mehrzahl der Patienten unzureichend (82 % bzw. 90 %). Bei den Patienten, die das Proteinziel nicht erreichten, wurden zudem mehr Clavien-Dindo-III-Komplikationen beobachtet [9].
Metabolische Risikopatienten sind vor allem die mit Resektionen am oberen Gastrointestinaltrakt. Bei Anastomosen nach Ösophagusresektion oder Gastrektomie besteht traditionell Zurückhaltung einer frühen oralen Nahrungszufuhr. In einer randomisierten multizentrischen niederländischen Studie wurden Machbarkeit und Sicherheit einer frühen oralen Nahrungszufuhr nach minimal invasiver Ösophagusresektion mit intrathorakaler Anastomose untersucht [10]. In der Interventionsgruppe (n = 65) erfolgte der orale Kostaufbau ohne Verzögerung, während die Kontrollgruppe für fünf Tage ausschließlich enteral über eine Sonde ernährt wurde (n = 67). Ein Unterschied in dem primären Endpunkt der postoperativen Erholung (sieben vs. acht Tage) und den sekundären Endpunkten Komplikationen, Anastomoseninsuffizienz (18.5 % vs. 16.4 %) und Pneumonierate (24.6 % vs. 34.3 %) wurde nicht beobachtet.
Aus ernährungsmedizinischer Sicht ist die orale Nahrungsaufnahme auch bei diesen Patienten „machbar”. Jedoch wird der Energiebedarf über eine längere Zeit auch noch nach der Entlassung nicht adäquat abgedeckt werden können. Dies wird als „bariatrischer Effekt” der Operation zu einem Gewichtsverlust führen und kann ein klares Argument für eine orale Supplementierung mit Trinknahrung oder sogar enteral über eine bei der Operation platzierte Nasojejunalsonde oder Feinnadelkatheterjejunostomie (FKJ) sein.
Enterale Ernährung über Feinnadelkatheterjeunostomie
Der Nutzen der Feinnadelkatheterjejunostomie vor allem nach Resektionen am oberen Gastrointestinaltrakt, mit der auch eine poststationär ambulante enterale Ernährung möglich ist, wird immer wieder kontrovers diskutiert. Retrospektiv haben Zhuang et al [11] von 716 Patienten mit Ösophagusresektion 68 mit intraoperativ platzierter Jejunostomiesonde mit den 648 Patienten ohne Sonde verglichen. Die Ernährungssonde wurde nur bei den Patienten implantiert, bei denen das Risiko einer Anastomoseninsuffizienz als hoch eingeschätzt wurde. Hinsichtlich der Krankenhausaufenthaltsdauer, der Letalität und des Gesamtüberlebens wurde kein signifikanter Unterschied beobachtet. Bei den Patienten mit Sonde bestand jedoch eine Tendenz zur rascheren Heilung einer Anastomoseninsuffizienz (27,2 vs. 37,4 d, p = 0,073). Sondenkomplikationen wurden nicht beobachtet.
Nasojejunalsonde vs. Feinnadekatherjejunostomie
Eine Metaanalyse von zehn Studien zum Vergleich von Jejunostomie versus Nasoenteralsonde zeigte Vorteile der Jejunostomie hinsichtlich postoperativer Pneumonie, Krankenhausverweildauer und Sondendislokation, jedoch bei erhöhtem Risiko für einen Ileus [12]. Ähnliche Ergebnisse erbrachte die retrospektive Analyse von 847 Patienten mit Ösophaguresektion aus dem Nationalen Schwedischen Register für Ösophagus- und Magenkarzinome. Im Falle einer Anastomoseninsuffizienz war das Risiko, schwere Komplikationen (Clavien-Dindo > IIIb) zu entwickeln, bei den Patienten mit Jejunostomie signifikant geringer. Das Risiko für zusätzliche Komplikationen durch die Jejunostomie war nicht erhöht [13]. So gibt es durchaus Argumente zumindest für einen selektiven Einsatz bei Hochrisikopatienten mit Ösophagsuresektion. [14]. Da jedoch die präoperative Einschätzung unzuverlässig sein kann, erfolgt im eigenen Patientengut die Implantation routinemäßig bei Patienten mit Ösophgusresektion, Gastrektomie und auch partieller Duodenopankreatektomie.
Indikation zur parenteralen Ernährung – der definitive Plan B
Die Good Clinical Practice Empfehlung der ESPEN-Leitlinie lautet: Wenn die orale und enterale Energie- und Nährstoffzufuhr für mehr als sieben Tage nicht mehr als 50 % des Bedarfs decken kann, wird die Kombination der enteralen mit einer parenteralen Ernährung empfohlen [2]. Im klinischen Alltag kann dies als vorübergehende Supplementierung auch bei weitgehend unkomplizierten Verläufen nach großen abdominellen Operationen zutreffen. Hierbei kann die Applikation bei eingeschränkter Kalorienzufuhr und Osmolarität auch peripher erfolgen.
Für die parenterale Ernährung des Intensivpatienten gibt es aktuelle Leitlinienempfehlungen der Deutschen Gesellschaft für Ernährungsmedizin e. V., die zwischen Akut- und Postakut- mit Rekonvaleszenz- und chronischer Phase differenzieren [15]. Diese sehen für die Substratzufuhr pro Tag folgende Höchstgrenzen vor: Glukose 4 g/kg Körpergewicht, Lipide 1,5 g/kg und Aminosäuren 1,2 g/kg [15].
Ernährung nach längerer Intensivbehandlung
Nach Verlegung von der Intensivstation ist die spontane orale Nahrungsaufnahme für längere Zeit zumeist unzureichend. Ursachen sind vor allem Inappetenz und auch Fatigue bei manchmal eingeschränkter Kooperation. Da sich nach schwerer Katabolie eine anabole Stoffwechsellage einstellt, ist die Unterversorgung mit Energie und Protein ein „metabolisches Dilemma“ und verstärkt noch das bestehende Defizit mit ungünstigen Auswirkungen auf die längerfristige Rehabilitation.
In einer kleinen Kohortenstudie wurden 32 Patienten nach der Verlegung von der Intensivstation mit ihrer Nahrungszufuhr gemessen am Energie- (2000; 1650–2550 kcal/d) und Proteinbedarf (112; 84–129 g/d) nachbeobachtet. Über 227 Tage wurden im Median 1238 (869–1813) kcal/d und 60 (35–89) g Protein aufgenommen. Die meisten Patienten wurden ausschließlich oral (55 %) oder kombiniert enteral (42 %) ernährt. Hierbei waren die Energie- und Proteinzufuhr niedriger als der geschätzte oder sogar mittels indirekter Kalorimetrie gemessene Energiebedarf. Es zeigte sich, dass Energie- und Proteinbedarf nur in der Kombination von oraler und enteraler Ernährung erreicht werden konnten. Auch die Supplementierung einer oralen Ernährung mit einer Trinknahrung deckte nur etwa 70 % des Bedarfs [16].
Poststationäre Supplementierung – wenn die Ernährungsberatung nicht ausreicht
Bereits erwähnt wurde der nach Resektionen am oberen Gastrointestinaltrakt anhaltende Gewichtsverlust, der als unerwünschter „bariatrischer” Effekt angesehen werden kann. Die diätetische Beratung und die ernährungsmedizinische Verlaufskontrolle des Ernährungsstatus einschließlich der quantitativen Nahrungsaufnahme sind unerlässlich. Eine systematische Übersicht von 18 Studien hat bei Patienten nach Ösophagusresektion einen postoperativen Gewichtsverlust von 5–12 % innerhalb von sechs Monaten gezeigt. Mehr als die Hälfte der Patienten verlor > 10 % an Körpergewicht [17]. In unserer eigenen Erfahrung muss nach Ösophagus- und Magenresektion, sowie partieller Duodenopankreatektomie auch bei poststationärer Fortsetzung einer enteralen Ernährungstherapie ein perioperativer Gewichtsverlust > 10 % bei 40 % der Patienten erwartet werden [18]. Koterazawa et al konnten ebenfalls zeigen, dass ein schwerer Gewichtsverlust drei Monate nach Ösophagusresektion durch eine enterale Ernährung nicht verhindert wird, dies jedoch signifikanten Einfluss auf die Prognose mit der 5-Jahres-Überlebensrate haben kann [19].
Die Leitlinien empfehlen für diese metabolischen Risikopatienten bei der Operation die Implantation einer Ernährungssonde, wobei die Feinnadelkatheterjejunostomie (FKJ) die Möglichkeit der längerfristigen auch poststationären Supplementierung bietet [2]. Zur Frage, ob dies nicht auch mit einer oralen Trinknahrung erreicht werden kann, ist bei der Einnahme von Trinknahrungen häufig eine eingeschränkte Compliance zu erwarten [20, 21]. Diese resultiert auch aus den „bariatrischen Effekten” der Operation mit Appetitverlust, Geschmack, Aufstoßen, Blähungen und Diarrhoe.
Trinksupplemente vs. enterale Ernährung
In einer aktuellen Metaanalyse von 15 randomisierten kontrollierten Studien mit 1059 Patienten mit Resektionen am oberen Gastrointestinaltrakt wurden heimenterale Ernährung und orale Trinksupplemente (ONS) verglichen [22]. Bei der heimenteralen Ernährung wurde im Vergleich zur Kontrolle ohne Supplementierung ein signifikant geringerer Gewichtsverlust (-3,95 vs –5,82 kg; SMD: 1,98 kg; 95 % CI 1,24–2,73) mit Verminderung der Entwicklung einer Mangelernährung beobachtet (RR = 0.54; p < 0,01). Keine signifikanten Unterschiede wurden hingegen im Vergleich zwischen den Patienten mit oraler Supplementierung und der Kontrollgruppe ohne Supplementierung gefunden. In der enteral ernährten Gruppe fielen auch die Dimensionen der Lebensqualität Körperliche Funktion und Fatigue signifikant besser aus.
In einer randomisierten Studie konnte bei 353 Patienten mit Nutrition Risk Score (NRS) > 3, die nach Gastrektomie in der Interventionsgruppe eine Ernährungsberatung in Kombination mit ONS erhielten, eine signifikante Verminderung des Gewichtsverlusts bei höherem Körper- (BMI) und Skelettmuskelindex (SMI) beobachtet werden. Während kein Unterschied in der 90-Tage-Wiederaufnahmerate bestand, waren Fatigue und Appetitverlust weniger häufig als bei den Patienten mit ausschließlicher Ernährungsberatung [23].
In einer multizentrischen randomisierten Studie von 1003 Patienten nach Gastrektomie wurden die Auswirkungen der Einnahme einer Trinknahrung mit 400 kcal/d auf den Gewichtsverlust nach einem Jahr mit Kontrollpatienten verglichen. Insgesamt war der Gewichtsverlust in der Interventionsgruppe nach drei Monaten signifikant geringer. Dies glich sich im weiteren Verlauf an und war nach einem Jahr ohne signifikanten Unterschied. In der ONS Gruppe nahmen nur 50.4 % der Patienten mehr als 200 kcal/Tag ein (im Mittel 301 ml), hatten aber nach einem Jahr einen signifikant niedrigeren Verlust des Körpergewichts (8,2 ± 7,2 %) als die Kontrollen (p = 0,0204) [24].
In der Zusammenschau kann davon ausgegangen werden, dass gerade nach Resektionen am oberen Gastrointestinaltrakt die postoperative orale/enterale Supplementierung in den ersten Monaten durchaus metabolische Vorteile für den weiteren Verlauf bietet – insbesondere bei Patienten mit Indikation zur adjuvanten/palliativen (Radio-)/Chemotherapie. Es fehlen jedoch noch mehr Daten zur Therapietoleranz und Patient Reported Outcomes (PROMS).
Zusammenfassung
- Im ERAS-Protokoll ist postoperativ das Ziel der frühe orale Kostaufbau
- Die traditionelle Schonung des Gastrointestinaltrakts einschließlich der Anastomosen kann Verlauf und Erholung verzögern
- Die Beobachtung von Nahrungszufuhr und Toleranz ist unerlässlich
- Die enterale und parenterale Supplementierung bietet gerade bei bereits präoperativ identifizierten Risikopatienten eine Ergänzung der primär oralen Ernährung, sofern hierdurch Kalorien- und Proteinbedarf nicht adäquat gedeckt werden können
- Insbesondere bei Patienten mit perioperativer enteraler und / oder supplementierender parenteraler Ernährungstherapie kann eine poststationäre Fortsetzung erforderlich sein.
Die Literaturliste erhalten Sie auf Anfrage per E-Mail an: passion_chirurgie@bdc.de
Weimann, A: Postoperative Ernährung. Passion Chirurgie. 2021 Dezember; 11(12): Artikel 03_03.
Autor:in des Artikels
Weitere aktuelle Artikel
10.02.2026 BDC|News
Passion Chirurgie 01/02-2026: Perioperatives Management
erioperatives Management steht im Fokus der Januar/Februar-Ausgabe. Drei Fachbeiträge beleuchten das Thema – von den zehn wichtigsten Maßnahmen im perioperativen Management, über den idealisierten Workflow im Zentral-OP bis hin zur Prähabilitation zwischen theoretischem Anspruch und praktischer Umsetzung. Viel Spaß beim Lesen!
20.01.2026 Fachübergreifend
Prähabilitation – vom theoretischen Ideal zur praktischen Umsetzung
Lange wurde dem Allgemeinzustand von Patient:innen vor onkologischen Eingriffen wenig Aufmerksamkeit geschenkt. Es galt die Devise, den Tumor so rasch wie möglich nach Diagnosestellung zu entfernen.
20.01.2026 Fachübergreifend
Prozessmanagement – Der idealisierte WorKFlow in einem Zentral-OP
Der idealisierte Workflow im Zentral-OP ergibt sich aus einer hochgradig standardisierten und zunehmend digital orchestrierten Prozesslandschaft.
20.01.2026 Fachübergreifend
Perioperatives Management – das sind die 10 wichtigsten Maßnahmen
In der modernen Chirurgie spielen viele Maßnahmen bezüglich eines adäquaten prä-, intra- und postoperativen Managements eine relevante Rolle, um die Krankenhausverweildauer sowie die Morbidität und Mortalität der Patient:innen zu reduzieren.
Lesen Sie PASSION CHIRURGIE!
Die Monatsausgaben der Mitgliederzeitschrift können Sie als eMagazin online lesen.