01.04.2026 Thoraxchirurgie
Vom Pleuraerguss zum Pleuraempyem – Diagnostik und Therapie im chirurgischen Alltag
Ein Pleuraerguss kombiniert mit klinischen Infektionszeichen ist charakteristisch für einen parapneumonischen Erguss (PPE), der die häufigste Ursache für ein Pleuraempyem darstellt. Die Inzidenz dieser pleuralen Infektionen ist ansteigend und stellt ein zunehmend klinisch relevantes Krankheitsbild dar, welches eine differenzierte Abklärung und Behandlung erfordert. Beim Pleuraempyem werden weiterhin abhängig vom Krankheitsstadium und den Vorerkrankungen des Patienten:in hohe Mortalitätsarten zwischen 6 % bis 35 % berichtet [1].
Pathophysiologie
Zur Klassifizierung des Krankheitsstadiums können drei verschiedene Systeme genutzt werden, die sich in der Stadieneinteilung ähneln.
Die Light-Kriterien beschreiben in sieben Stufen die Entwicklung vom nicht-signifikanten PPE bis hin zum komplexem Pleuraempyem auf der Grundlage von laborchemischen, radiologischen und physikalischen Parametern (Abb. 1) [2]. Gemäß der British Thoracic Society (BTS) erfolgt eine Differenzierung zwischen dem unkompliziertem PPE (UPPE = klares Punktat, keine Septierungen, pH-Wert > 7,2, LDH < 1000 IU/l, Glukose > 40 mg/dl), dem komplizierten PPE (CPPE = trübes/purulentes Punktat, häufig Septierungen, pH-Wert < 7,2, LDH > 1000 IU/l, Glukose < 40 mg/dl) und dem klassischen Pleuraemypem (purulentes Punktat, häufig Keimnachweis) (Abb. 1) [3]. Die klinische Stadieneinteilung sowie die adaptierte chirurgische Therapie richtet sich vornehmlich an die ATS-Klassifikation (American Thoracic Society), welche gemäß dem pathophysiologischen Verlauf einen fließenden Übergang zwischen der exsudativen (I), der fibrino-purulenten (II) und der Organisationsphase (III) unterscheidet [4].
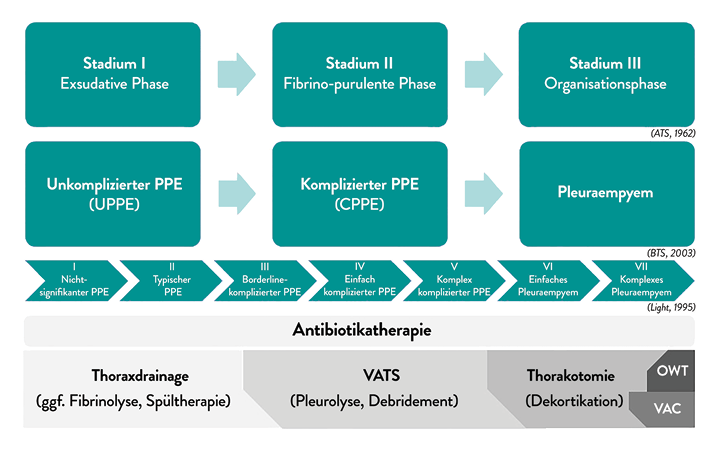
Abb. 1: Stadien-adaptierte Therapie des PPE bis hin zum Pleuraempyem (VAC= Vacuum-Assisted Closure; OWT= Open Window Thoracostomy); modifiziert nach [10, 11].
Klinisches Bild und Diagnostik
Die klinische Vorstellung von Patienten:innen mit einem PPE oder Pleuraempyem erfolgt meist mit unspezifischen Symptomen wie Husten, Fieber, thorakalen bzw. pleuritischen Schmerzen und Dyspnoe. Zudem sollte bei wiederauftretendem Fieber oder respiratorischer Verschlechterung ein bis zwei Wochen nach Behandlung einer Pneumonie an ein PPE bzw. Pleuraempyem gedacht werden und entsprechende Patient:innen auf einen potentiellen PPE untersucht werden. Bei einer Pneumonie ohne initialen Nachweis eines Pleuraergusses kann sich im Verlauf in bis zu 57 % der Fälle ein PPE bilden, weshalb entsprechende Kontrollen (Sonographie, Röntgen, CT) erfolgen sollten [5]. Insbesondere auch postoperativ (z. B. prolongierte Parenchymfistelung, bronchiale oder ösophageale Anastomoseninsuffizienz, Bronchusstumpfinsuffizienz) sollte bei jeder unklaren Sepsis mit Thoraxschmerz an die Möglichkeit einer mediastinalen oder pleuralen Infektion gedacht werden.
Entscheidend für den Therapieerfolg ist eine zügige und zielgerichtete Diagnostik, die eine frühe Differenzierung zwischen unkomplizierten und komplizierten PPE und einem Pleuraempyem ermöglicht (Abb. 2). Die Indikation für ein Kontrastmittel-CT des Thorax besteht bei ausbleibender Besserung unter der Pneumonie-Therapie oder komplexen Pleuraergüssen. Hierbei weisen abgekapselte Ergussanteile sowie das „split-pleura-sign“ auf einen komplizierten PPE oder bereits auf ein Pleuraempyem hin. Lufteinschlüsse im Verhalt sind pathognomonisch [6].
Eine sofortige Abklärung eines Pleuraergusses ist erforderlich bei:
- persistierendem oder erneutem Fieber > 48 h unter Antibiotika
- Sepsis mit unklarem Fokus
- einseitigem Thoraxschmerz oder Dyspnoe bei Pneumonie
- sonographisch septiertem oder echogenem Pleuraerguss
- Hinweise auf Ösophagusperforation oder Infekt nach thorakalem Eingriff
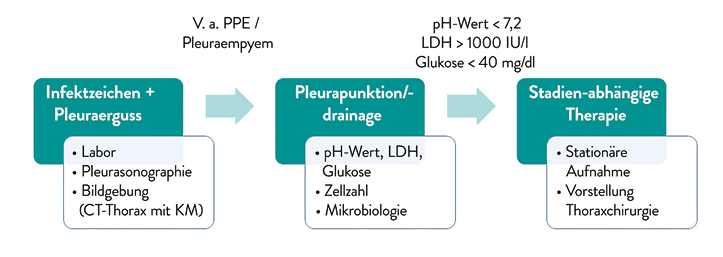
Abb. 2: Diagnostisches Vorgehen beim PPE bis hin zum Pleuraempyem.
Therapieprinzipien
Die Therapie des PPE bzw. Pleuraempyems basiert auf drei Säulen [6]:
- Kontrolle der Infektion
- Drainage bzw. Entfernung des infizierten Ergusses und Gewebes
- Re-Expansion der Lunge
Die Therapie sollte immer Stadien-adaptiert und dem klinischen Zustand des Patienten:in angepasst erfolgen (Abb. 1) [7–10]. Anwendung finden lokale (v. a. Drainage, Operation) und zugleich systemische (v. a. Antibiotikatherapie) Maßnahmen. Eine empirische Antibiotikatherapie sollte frühestmöglich initiiert werden und neben klassischen Pneumonie-Erregern (grampositive Aerobier) auch Anaerobier abdecken. Bei positiven Erregernachweis ist die Antibiotikatherapie dem Antibiogramm anzupassen. Die Dauer der Antibiotikagabe ist individuell und richtet sich nach den klinischen und laborchemischen Parametern. Empfohlen wird eine intravenöse Antibiotikatherapie für mindestens fünf bis sieben Tage, gefolgt von einer oralen Antibiotikagabe über weitere ein bis zwei Wochen in Abhängigkeit vom klinischen Verlauf und den Entzündungsparametern. Ein engmaschiges Monitoring von Drainagefunktion (Fördermenge, Ergussqualität), Fieberverlauf und laborchemischen Entzündungswerten ist unerlässlich.
Die sonographisch gesteuerte Anlage einer möglichst weitlumigen Thoraxdrainage (ggf. Spül-Saugdrainage) ist zur Evakuierung bzw. Entlastung des pleuralen Verhaltes v. a. beim UPPE und einem Pleuraempyem Stadium I indiziert. Insbesondere ab einem pH-Wert < 7,2 ist die Thoraxdrainagenanlage angezeigt [2, 7]. Bei nicht operationsfähigen Patient:innen und frustraner Drainagebehandlung kann der Einsatz von intrapleuralen Fibrinolytika erwogen werden. Aktuell ist das therapeutische Regime (DNAse + tPA) jedoch nur im Off-Label-Use anwendbar. Weiter ist zu bedenken, dass die routinemäßige Behandlung mit Fibrinolytika die chirurgische Behandlung möglicherweise verzögert. Bleibt die Symptomatik nach 48 bis 72 Stunden unter adäquater Drainage unverändert oder zeigt sich im CT ein nicht drainierter Erguss, muss bei diesen Patienten die operative Therapie erneut diskutiert werden.
Bei der operativen Therapie wird zwischen dem chirurgischen Debridement (= Entfernung von entzündlichem und nekrotischem Gewebe im Pleuraraum) und der Dekortikation (= Entfernung der entzündlich veränderten viszeralen und/oder parietalen Pleura) differenziert, wobei beide Maßnahmen abhängig vom Erkrankungsstadium Anwendung finden. Die video-assistierte Thorakoskopie (VATS) ist abhängig vom Stadium und der pleuralen Ausprägung der bevorzugte operative Zugang (Abb. 3). Das minimal-invasive Vorgehen bietet gegenüber einer Thorakotomie die bekannten Vorteile einer geringeren Morbidität und Mortalität, kürzeren Verweildauer und besseren Lebensqualität [11].
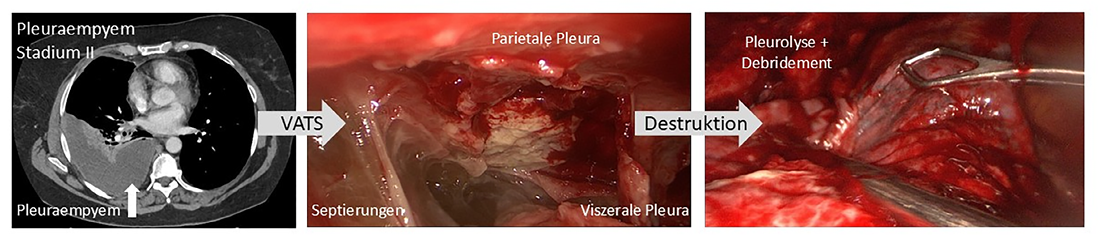
Abb. 3: Thorakoskopische Destruktion bei Pleuraemypem Stadium II.
Beim CPPE bzw. beim Pleuraempyem in den Stadien II und III ist die thoraxchirurgische Destruktion mit den Zielen einer vollständigen Evakuierung des infizierten pleuralen Gewebes und der Wiederherstellung der Lungenexpansion zur Vermeidung einer Resthöhlenbildung sowie Verbesserung der Lungenfunktion durchzuführen [12]. Eine Verzögerung der Operation erschwert die vollständige Dekortikation und erhöht die Komplikations- sowie Mortalitätsrate. Pleuraempyeme in fortgeschrittenen Stadien II-III erfordern aufgrund der pleuralen Schwartenbildung i. d. R. eine Thorakotomie zur möglichst vollständigen Dekortikation (Abb. 4). Bei schwer vorerkrankten oder für komplexere Eingriffe inoperablen Patienten:innen bieten sich spezielle Verfahren wie insbesondere die intrathorakale Vakuumtherapie als therapeutisches Verfahren an [13].
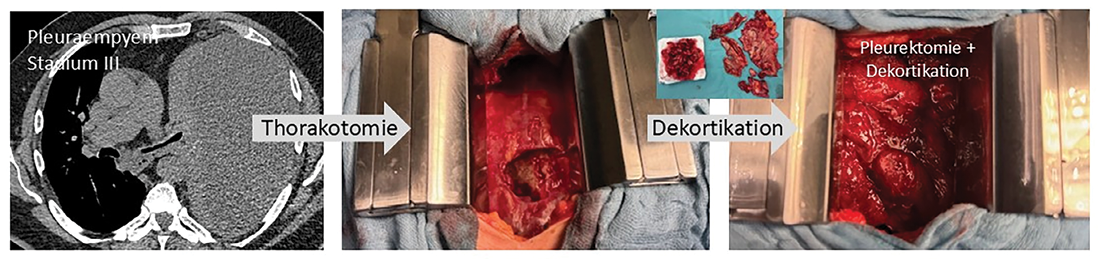
Abb. 4: Offene Dekortikation bei Pleuraempyem Stadium III.
Fazit
Das Pleuraempyem ist ein häufig unterschätztes, aber potenziell lebensbedrohliches Krankheitsbild. Entscheidend für den Therapieerfolg sind die frühzeitige, differenzierte Diagnostik und ein stadien-adaptiertes Behandlungskonzept. Die Drainage ist beim komplizierten PPE unverzichtbar. Bei unzureichender Entlastung muss frühzeitig die thoraxchirurgische, operative Versorgung erfolgen.
Literatur
[1] Bedawi EO, Ricciardi S, Hassan M, Gooseman MR, Asciak R, Castro-Añón O, Armbruster K, Bonifazi M, Poole S, Harris EK, Elia S, Krenke R, Mariani A, Maskell NA, Polverino E, Porcel JM, Yarmus L, Belcher EP, Opitz I, Rahman NM. ERS/ESTS statement on the management of pleural infection in adults. Eur Respir J. 2023 Feb 2;61(2):2201062. doi: 10.1183/13993003.01062-2022. PMID: 36229045
[2] Light RW. A new classification of parapneumonic effusions and empyema. Chest. 1995 Aug;108(2):299-301. doi: 10.1378/chest.108.2.299. PMID: 7634854.
[3] Davies HE, Davies RJ, Davies CW; BTS Pleural Disease Guideline Group. Management of pleural infection in adults: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010 Aug;65 Suppl 2:ii41-53. doi: 10.1136/thx.2010.137000. PMID: 20696693.
[4] Andrews N, Parker E, Shaw R, Wilson N, Webb W. Management of nontuberculous empyema. A statement of the ATS subcommittee on surgery. Am Rev Respir Dis; 1962.
[5] Dean NC, Griffith PP, Sorensen JS, McCauley L, Jones BE, Lee YC. Pleural Effusions at First ED Encounter Predict Worse Clinical Outcomes in Patients With Pneumonia. Chest. 2016 Jun;149(6):1509-15. doi: 10.1016/j.chest.2015.12.027. Epub 2016 Jan 16. PMID: 26836918; PMCID: PMC6026265.
[6] Hecker E, Hecker HC, Hecker KA. Pleuraempyem – Behandlungsstrategien unter Berücksichtigung der Ätiologie [Pleural empyema – treatment strategies in light of etiology]. Zentralbl Chir. 2013 Jun;138(3):353-77; quiz 378-9. German. doi: 10.1055/s-0032-1328638. Epub 2013 Jun 27. PMID: 23807591.
[7] Roberts ME, Rahman NM, Maskell NA, Bibby AC, Blyth KG, Corcoran JP, Edey A, Evison M, de Fonseka D, Hallifax R, Harden S, Lawrie I, Lim E, McCracken D, Mercer R, Mishra EK, Nicholson AG, Noorzad F, Opstad KS, Parsonage M, Stanton AE, Walker S. British Thoracic Society Guideline for pleural disease. Thorax. 2023 Nov;78(11):1143-1156. doi: 10.1136/thorax-2023-220304. Epub 2023 Aug 8. PMID: 37553157.
[8] Reichert M, Hecker M, Witte B, Bodner J, Padberg W, Weigand MA, Hecker A. Stage-directed therapy of pleural empyema. Langenbecks Arch Surg. 2017 Feb;402(1):15-26. doi: 10.1007/s00423-016-1498-9. Epub 2016 Nov 4. PMID: 27815709.
[9] Shen KR, Bribriesco A, Crabtree T, Denlinger C, Eby J, Eiken P, Jones DR, Keshavjee S, Maldonado F, Paul S, Kozower B. The American Association for Thoracic Surgery consensus guidelines for the management of empyema. J Thorac Cardiovasc Surg. 2017 Jun;153(6):e129-e146. doi: 10.1016/j.jtcvs.2017.01.030. Epub 2017 Feb 4. PMID: 28274565.
[10] Hofmann HS. Modern management of empyema thoracis. Semin Thorac Cardiovasc Surg. 2013 Winter;25(4):287-91. doi: 10.1053/j.semtcvs.2013.07.006. PMID: 24673957.
[11] Ried M, Graml J, Großer C, Hofmann HS, Sziklavari Z. Para- and Postpneumonic Pleural Empyema: Current Treatment Strategies in Children and Adults. Zentralbl Chir. 2015 Oct;140 Suppl 1:S22-8. German. doi: 10.1055/s-0035-1557771. Epub 2015 Sep 9. PMID: 26351760.
[12] Potzger T, Ried M, Hofmann HS. Dekortikation bei Pleuraempyem: funktionell sinnvoll? [Decortication in Pleural Empyema: Reasonable Effects on Lung Function?]. Zentralbl Chir. 2016 Sep;141 Suppl 1:S18-25. German. doi: 10.1055/s-0042-112025. Epub 2016 Sep 8. PMID: 27607885.
[13] Sziklavari Z, Hammoudeh S, Petrone AM, Stange S, Orban K, Fekete JT, Hofmann HS. Outcomes of Vacuum-Assisted Closure in Patients with Empyema Thoracis: A 10-Year Experience. Ann Thorac Surg. 2025 Jun;119(6):1206-1212. doi: 10.1016/j.athoracsur.2024.08.003. Epub 2024 Aug 22. PMID: 39178929.

Korrespondierender Autor:
Dr. med. Dominik Herrmann
Klinik für Thoraxchirurgie
Evangelisches Krankenhaus Herne

Dr. med. Dipl.-Oec. Erich Hecker
Klinik für Thoraxchirurgie
Evangelisches Krankenhaus Herne

Prof. Dr. med. Hans-Stefan Hofmann
Abteilung für Thoraxchirurgie
Universitätsklinikum Regensburg
Klinik für Thoraxchirurgie
Krankenhaus Barmherzige Brüder Regensburg

Prof. Dr. med. Michael Ried
Abteilung für Thoraxchirurgie
Universitätsklinikum Regensburg
Chirurgie
Herrmann D, Hecker E, Hofmann HS, Ried M: Vom Pleuraerguss zum Pleuraempyem – Diagnostik und Therapie im chirurgischen Alltag. Passion Chirurgie. 2026 April; 16(04): Artikel 03_04.
Weitere aktuelle Artikel
01.01.2019 Thoraxchirurgie
Beste Karrierechancen in der Viszeralchirurgie und in der Thoraxchirurgie
Die Schwierigkeiten, ärztliche Führungspositionen zu besetzen, nehmen zu. Wollen Krankenhäuser heutzutage eine Oberarztstelle besetzen, brauchen sie häufig einen langen Atem. Dass Vakanzen auf der zweiten Führungsebene länger als ein Jahr bestehen bleiben, ist keine Seltenheit mehr. Und auch Chefarztbesetzungen laufen in einigen Bereichen nicht mehr ganz reibungslos.
09.10.2017 BDC|News
Passion Chirurgie: Thoraxchirurgie
Pleura, Lunge, Tracheo-Bronchialsystem, Mediastinum und Thoraxwand sind „Spielfelder“ der aktuellen Ausgabe PASSION CHIRURGIE: Die Thoraxchirurgie steht im Fokus. Denn in diesem Monat findet die 26. Jahrestagung der Deutschen Gesellschaft für Thoraxchirurgie (DGT) unter dem Schlagwort „Horizonte“ in München statt. Gerade für ein kleines, aber hoch spezialisiertes Fachgebiet wie die Thoraxchirurgie ist die Kooperation mit anderen chirurgischen Disziplinen wichtig.
01.10.2017 Aus- & Weiterbildung
Berufspolitische Themen im Fachbereich Thoraxchirurgie
diejenigen unter Ihnen, die bereits Mitglieder im BDC sind, haben offensichtlich im Rahmen einer Entscheidungsfindung erkannt, wie wichtig aktive Berufspolitik ist. Der BDC ist der größte chirurgische Berufsverband in Europa. Da drängt sich zwangsläufig die Frage auf, welche spezifischen Themen im Referat Thoraxchirurgie für eine zahlenmäßig vergleichsweise kleine Berufsgruppe als relevant erachtet werden.
01.10.2017 Thoraxchirurgie
Thoraxchirurgie gestern und heute
Die Anfänge der Thoraxchirurgie liegen nicht nur in den Händen großer chirurgischer Vorväter wie von Langenbeck, Billroth, Nissen oder Sauerbruch, sondern auch in denen von Internisten, die sich mit den Möglichkeiten der Behandlungen der Tuberkulose durch gezielte Anlage eines Pneumothorax beschäftigten.
Lesen Sie PASSION CHIRURGIE!
Die Monatsausgaben der Mitgliederzeitschrift können Sie als eMagazin online lesen.