Problemstellung
Die Diagnostik und Therapie muskuloskelettaler Tumoren stellt für die involvierten Ärzte des Behandlungsteams eine besondere Herausforderung dar. Es ist von vitaler Bedeutung aus dem „Potpourri“ der verschiedenen radiologischen Darstellungsformen von Knochen- und Weichgewebstumoren die muskuloskelettalen Malignome zu detektieren. Während die benignen bzw. tumorähnlichen Läsionen häufig als Zufallsbefund in der bildgebenden Diagnostik registriert werden und ein symptomorientiertes Vorgehen nach dem „wait and watch“ Prinzip erlauben, erfordert das Vorliegen eines muskuloskelettalen Malignoms eine rasche, zielgerichtete Diagnostik und Initiierung der optimalen Therapie [1, 2].
Erschwert wird dieser medizinische Anspruch durch die geringe Inzidenz der primär malignen Knochen- und Weichgewebstumoren von einem Prozent im Erwachsenenalter und sechs bzw. zehn Prozent im Kindesalter [3]. Folglich wird ein niedergelassener Chirurg bzw. Orthopäde im Durchschnitt alle drei Jahre in seiner Praxis mit einem Knochentumor konfrontiert. Diese epidemiologische Besonderheit verbunden mit Unsicherheiten der dignitätsspezifischen Einordnung führt einerseits zu einer Überdiagnostik benigner Läsionen, andererseits ist die Diagnostik muskuloskelettaler Malignome durch Fehlinterpretation der Symptome leider immer noch unnötig protrahiert. Während die durch den Patienten selbst bedingte Verzögerung der Tumordiagnose nach Symptombeginn einen Monat beträgt, addieren sich im Durchschnitt noch drei Monate durch ärztliche Verzögerung der Diagnostik hinzu [4]. Diese summierte Diagnoseverzögerung mit konsekutiv vergrößertem Tumorvolumen führt zu einer vermeidbaren Prognoseverschlechterung [5]. Hieraus resultiert das übergeordnete Ziel, das diagnostische Intervall möglichst klein zu halten.
Durch Zusammenführen diagnostischer und therapeutischer Kompetenz in einem interdisziplinären Behandlungsteam kann diesen besonderen Anforderungen in der Behandlung muskuloskelettaler Tumoren am besten entsprochen werden [6].
Definition des interdisziplinären Behandlungsteams
Der diagnostische Algorithmus und die therapeutische Sequenz von Knochen- und Weichgewebstumoren erfordert die Formation von interdisziplinären Behandlungsteams bestehend aus muskuloskelettal orientierten Radiologen und Pathologen, Chirurgen unterschiedlicher Schwerpunkte, sowie Onkologen und Strahlentherapeuten zur Einbindung multimodaler Behandlungskonzepte [7]. Diese Struktur ist in erster Linie in onkologischen Zentren zu finden, wo die interdisziplinäre Arbeit der Behandlungsteams in wöchentlich abgehaltenen Tumorkonferenzen gelebt wird. Während die numerisch dominierenden Karzinome in Organzentren behandelt werden, sind die seltenen Knochen- und Weichgewebssarkome meistens als universitärer Schwerpunkt in regionalen Sarkomzentren organisiert. Diese sollten als Referenzzentrum fungieren, in der die interdisziplinär verortete Expertise zusammengeführt und das vorhandene Wissen aufbereitet u. a. bei externen Anfragen kollegial zur Verfügung gestellt wird. D. h. Behandlungsteams sind nicht ausschließlich monoinstitutionell, sondern auch transsektorial als Verzahnung von ambulanter und stationärer Versorgung zu begreifen. Das Behandlungsteam sollte nicht an der Klinikumspforte beginnen oder enden, sondern als kollegiales Kompetenznetzwerk unter Einbindung niedergelassener Chirurgen gelebt werden. Idealerweise zeichnet sich diese transsektoriale Zusammenarbeit durch Konzentration und Kommunikation von Wissen, Koordination der Diagnostik und Therapie, chirurgische und onkologische Kooperation, Kontinuität in der Behandlung und Nachsorge sowie Kollegialität zwischen niedergelassenen und Klinik- Ärzten aus [8].
Rolle des Chirurgen als Diagnostiker und Operateur
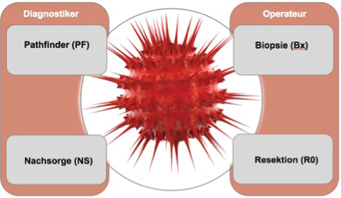
Im diagnostischen und therapeutischen Algorithmus muskuloskelettaler Tumoren nimmt der Chirurg eine Schlüsselrolle ein, die charakterisiert ist durch jeweils zwei diagnostische und operative Funktionen (Abb. 1).
Insbesondere kommt dem niedergelassenen Chirurgen die vordringliche Funktion als sog. „Türöffner“ für das Erkennen eines muskuloskelettalen Malignoms und Einleitung der korrekten Erstdiagnostik zu. Er fungiert also ganz wesentlich als „Pathfinder“ für die rasche initiale Weichenstellung des adäquaten diagnostischen Pfades.
Radiologische Diagnostik
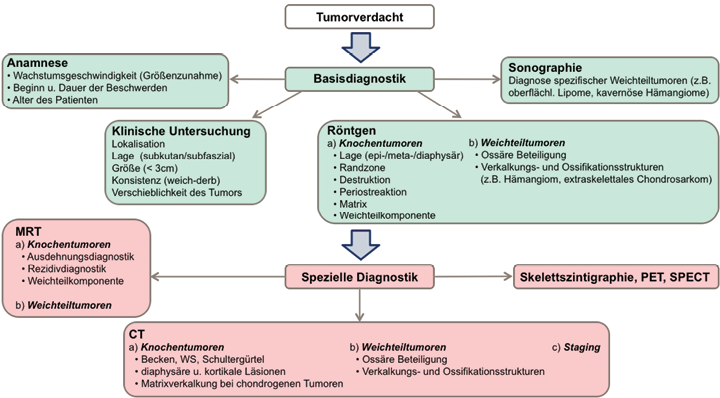
In der Diagnostik von Knochen- und Weichgewebstumoren wird in zwei sequentiellen Stufen zwischen der Basisdiagnostik und speziellen Diagnostik unterschieden (Abb.2). Initialer Bestandteil der Basisdiagnostik ist die genaue Anamnese von Beginn und Dauer der Beschwerdesymptomatik, Wachstumstendenz des Tumors sowie Patientenalter. Im Rahmen der klinischen Untersuchung wird Lokalisation, Lage, Größe, Verschieblichkeit und Konsistenz der Raumforderung erfasst. Für die Primärdiagnostik von Knochentumoren hat das konventionelle Röntgen nach wie vor uneingeschränkten Stellenwert [9].
Nachfolgende sechs röntgenmorphologische Kriterien sind unter Verwendung der konventionellen Projektionsradiographie zur entitäts- und dignitätsspezifischen Einordnung einer ossären Läsion zu beurteilen [10]:
1. Lage (epi-/meta-/diaphysär)
2. Randzone (scharf begrenzt mit oder ohne Sklerose/unscharf begrenzt)
3. Destruktion (geographische Osteolyse, Mottenfraß, permeative Osteolyse)
4. Matrix (osteoblastisch, chondroblastisch, transparent/osteolytisch)
5. Periostreaktion (Codman-Dreieck, Zwiebelschalen, Spiculae, sunburst sign)
6. Weichteilkomponente (vorhanden bei Zeichen einer Periostreaktion)
Das Vorhandensein einer Weichteilkomponente spricht für einen biologisch aggressiven Tumor.
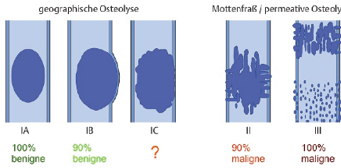
Anhand des röntgenmorphologischen Destruktionsmusters, welches nach Lodwick [11] in fünf Formen eingeteilt wird, kann eine zuverlässige Dignitätseinschätzung des Knochentumors erfolgen (Abb. 3) [12].
•Grad I beschreibt eine geographische Destruktion mit drei Subtypen :
– I a Läsion regulär lobuliert, scharf begrenzt, immer mit Sklerosesaum und ggf. Kompaktaausbeulung <1cm, klinisch meist asymptomatisch.
– I b Läsion regulär lobuliert, scharf begrenzt, Sklerosesaum und Kompaktaausbeulung >1cm möglich.
– I c Läsion regulär lobuliert, unscharf begrenzt, vollständige Kompaktapenetration.
•Grad II beschreibt die mottenfraßartige Destruktion als Ausdruck eines beschleunigten Wachstums der Läsion mit diskontinuierlicher Kompaktapenetration
•Grad III beschreibt die permeative Destruktion durch sehr schnelles Tumorwachstum mit totaler Kompaktapenetration
Biopsie
Die Biopsie ist als Gewebeentnahme aus einem lebenden Organismus definiert und dient – durch histopathologische, immunhistochemische und molekularpathologische Aufarbeitung im Kontext mit der zuvor veranlassten Bildgebung – der endgültigen Diagnosefindung.
Für eine repräsentative Biopsie sind Gewebeanteile aus proliferativ aktiven Arealen unerlässlich. Diese biologisch relevanten Gewebeareale als bösartigster Anteil eines Tumors liefern die korrekte histopathologische Diagnose nach der sich die adäquate Therapie ausrichtet. Dagegen wird eine zentral entnommene Biopsie viel nekrotisches Gewebe aufweisen, welches keine sichere histopathologische Diagnose bzgl. Entität, Grading und Dignität ermöglicht [13].
Es konnte in Studien wiederholt nachgewiesen werden, dass die mit einer Biopsie in Zusammenhang stehenden Komplikationen in spezialisierten Tumorzentren drei- bis fünfmal seltener sind als in allgemeinen Behandlungseinheiten [14].
Um die von der Biopsie ausgehenden Risiken für den Patienten zu minimieren, sind nachfolgende spezielle tumorchirurgische Richtlinien zu beachten [15]:
•Die Biopsie richtet sich nach dem geplanten Zugangsweg für die definitive Tumorresektion.
•Probenentnahme an der Extremität soweit distal wie möglich
•direkter Zugang zum Tumor über kürzesten Weg
•kein Unterfahren der Haut, keine Kulissenbildung
•kein Eröffnen zusätzlicher Kompartimente
•kein Eröffnen eines vom Tumor infiltrierten Gelenkes (maligne Ergussbildung)
•kein Darstellen von Gefäß-Nerven-Bündeln
•Der Biopsieweg folgt nicht den Standardzugängen.
•Vermeidung einer Hämatombildung durch akribische Blutstillung, Knochenwachs oder Zementplombe
•Ausleitung der Redondrainage im Verlauf des Hautschnittes nah am distalen Wundpol
Chirurgische Resektionsverfahren
Die operative Therapie von Knochen- und Weichgewebstumoren erfordert aufgrund ihrer Komplexität chirurgische Fertigkeiten, die nur über eine breit angelegte chirurgische Ausbildung nach „klassischem“ Weiterbildungsmuster erworben werden können. Gefragt ist kein „Single-Joint-Surgeon“ oder „Mikado-Chirurg“, sondern ein operativ versierter Chirurg, der aufgrund des topographischen Verteilungsmusters muskuloskelettaler Tumore zumindest sowohl in der Schulter/Oberarmregion als auch in der Becken/Oberschenkel- und Kniegelenksregion inklusive neurovaskulärer Präparation mit lokal-plastischer Deckungsmaßnahmen „zu Hause“ ist.
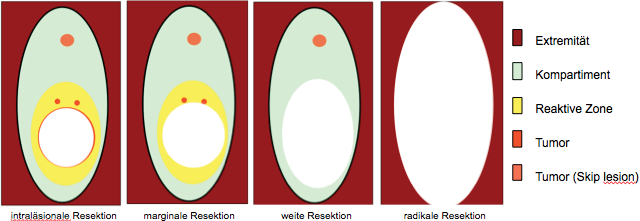
Neben Dignität des Tumors ist die genaue Kenntnis der Grenzzone von Tumor zu gesundem Gewebe entscheidend für die richtige Wahl des chirurgischen Resektionsverfahrens (Abb. 4) [16].
1. Intraläsionale Resektion: Entfernung des Tumors von innen heraus in mehreren Stücken wie z. B. durch Kürettage mit dem scharfen Löffel bis an die Grenzschicht heran. Teile der (Pseudo-) Kapsel verbleiben, sodass der Pathologe die komplette Entfernung des Tumors nicht beurteilen bzw. histologisch bestätigen kann (histopathologisch R1 bis R2). Sie kommt vorwiegend bei gutartigen Tumoren zu Anwendung, kann aber in indizierten Fällen auch bei niedrig-malignen Tumoren wie Chondrosarkom G1 oder Riesenzelltumoren plus Resektionsranderweiterung durch Hochfrequenzfräse und Applikation von Adjuvantien wie Knochenzement durchgeführt werden.
2. Marginale Resektion: Äußere Entfernung des Tumors entlang der (Pseudo-) Kapsel mit vollständiger Entfernung des eigentlichen Tumorgewebes ohne Eröffnung desselben. Möglicherweise bereits vorhandene Satelliten Absiedlungen in der reaktiven Zone würden verbleiben (histopathologisch R1). Bei Tumorwachstum mit aggressiver Biologie besteht die große Gefahr eines Lokalrezidivs. Diese Resektionsform kommt bei benignen (z. B. Lipomen, Myxomen) bzw. intermediären Tumoren wie z. B. atypischen lipomatösen Tumoren (ALT) zur Anwendung.
3. Weite Resektion: Enbloc Resektion des Tumors mit einer sicheren (idealerweise 2-3 cm) Schicht gesunden Gewebes als Überzug. Der gesamte Tumor ist von einer Schicht gesunden Gewebes umhüllt (histopathologisch R0). Diese Resektionsform ist das extremitätenerhaltende Standardverfahren für die operative Therapie von Knochen- und Weichteilsarkomen protokollarisch eingebunden in einem multimodalen radio-chemotherapeutischen Behandlungskonzept (z. B. Euro Ewing).
4. Radikale Resektion: Enbloc Resektion des Tumors unter Mitnahme des gesamten anatomischen Ausbreitungsraumes (Kompartiment), z. B. totale Femurresektion bei Nachweis sog. Skipläsionen. Aber auch für radikale Resektionsverfahren inklusive Amputationen gilt, dass die ungünstigste Schnittgrenze zum Tumor, sei sie noch so klein in ihrem Anteil bemessen, entscheidend für die weitere Prognose ist.
Die lokale Eliminierung des Tumors hat höchste Priorität. Der funktionelle Erhalt ist sekundäres Kriterium und sollte dem Ziel der weiten oder radikalen Resektion untergeordnet bleiben [17].
Nachsorge
Die Tumornachsorge von Patienten mit muskuloskelettalen Malignomen richtet sich nach der Tumorbiologie. Die Metastasierung bei Knochen- und Weichteilsarkomen erfolgt in der Regel hämatogen. Die Lunge zeigt aufgrund ihrer „zellulären Filterfunktion“ dabei mit 70 Prozent die häufigste Metastasenmanifestation, gefolgt vom Skelett mit 20 Prozent.
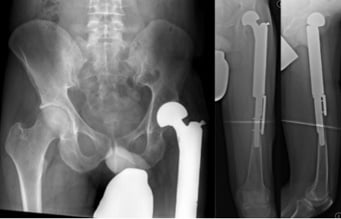
Die Rolle des Chirurgen beinhaltet einerseits die onkologische lokale Nachsorge zur Früherkennung eines Lokalrezidivs und andererseits bei Verwendung von Tumorprothesen zur Extremitätenrekonstruktion die langfristige endoprothetische Nachsorge zur rechtzeitigen Detektion biomechanischer Komplikationen (Abb. 5).
Als „Faustregel“ gelten für die Nachsorge von Sarkomen in den ersten 2 Jahren 3 monatliche Nachsorgeintervalle, bis zum fünften Jahr halbjährliche Kontrollen und danach bis zum zehnten Jahr jährliche Verlaufskontrollen, die mit denen im Gleichklang stattfindenden radio-onkologischen und hämato-onkologischen Nachsorgeuntersuchungen abgestimmt sind [18].
Fazit für die Praxis
•Die operative Rolle des Chirurgen in der Behandlung von muskuloskelettalen Tumoren wird flankiert von Schlüsselfunktionen in der Eingangsdiagnostik und Nachsorge von Tumoren.
•Eine genaue Anamnese zur Beschwerdesequenz und klinischer Symptomkonstellation helfen die Differenzialdiagnosen einzugrenzen.
•Das konventionelle Röntgenbild in zwei Ebenen hat weiterhin uneingeschränkten Stellenwert in der Primärdiagnostik von Knochentumoren.
•Die lokale und systemische Ausbreitungsdiagnostik sollte vor der Biopsie abgeschlossen sein.
•Die Biopsie ist der Endpunkt einer standardisierten diagnostischen Kaskade.
•Die Versorgungsrealität in Deutschland ist durch Fortbildung der niedergelassenen Erstversorger, schnelle Zuweisung an erfahrene Behandler und speziell ausgebildete muskuloskelettale Tumorchirurgen zu optimieren.
•Eingebettet im multimodalen Behandlungskonzept ist die weite Resektion das Standardverfahren für muskuloskelettale Malignome.
Literatur
[1] Enneking WF, Spanier SS, Goodman MA. Current concepts review. The surgical staging of musculoskeletal sarcoma. The Journal of bone and joint surgery. American volume 1980; 62:1027-1030.
[2] Pencavel TD, Strauss DC, Thomas GP, Thomas JM, Hayes AJ. Does the two-week rule pathway improve the diagnosis of soft tissue sarcoma? A retrospective review of referral patterns and outcomes over five years in a regional sarcoma centre. Ann RColl Surg Engl 2010; 92(5):417-421.
[3] Arora RS, Alston RD, Eden TO et al. The contrasting age-incidence patterns of bone tumours in teenagers and young adults: Implications for aetiology. International journal of cancer. Journal international du cancer 2012; 131:1678-1685.
[4] George A, Grimer R. Early symptoms of bone and soft tissue sarcomas: could they be diagnosed earlier? Ann R Coll Surg Engl 2012; 94(4):261-266.
[5] Grimer RJ, Briggs TW. Earlier diagnosis of bone and soft tissue tumours. J Bone Joint Surg Br 2010; 92(11):1489-1492.
[6] Ruhstaller T, Roe H, Thürlimann B, Nicoll JJ. The multidisciplinary meeting: An indispensable aid to communication between different specialities. Eur J Cancer 2006; 42:2459-2462.
[7] Lamb BW, Brown KF, Nagpal K, Vincent C, Green JS, Sevdalis N. Quality of care management decisions by multidisciplinary cancer teams: a systematic review. Ann Surg Oncol 2011; 18:2116-2125.
[8] Lamb BW, Taylor C, Lamb JN, Strickland SL, Vincent C, Green JS, Sevdalis N. Facilitators and barriers to teamworking and patient centeredness in multidisciplinary cancer teams: findings of a national study. Ann Surg Oncol 2013; 20: 1408-1416.
[9] Enneking WF, Spanier SS, Goodman MA (1980) Current concepts review. The surgical staging of musculoskeletal sarcoma. The Journal of bone and joint surgery. American volume 62:1027-1030.
[10] Freyschmidt J [Standards and diagnostic strategies in diagnosis of bone tumors and tumor-simulating lesions]. Der Radiologe 1998; 38:287-300.
[11] Lodwick GS, Wilson AJ, Farrell C et al. Determining growth rates of focal lesions of bone from radiographs. Radiology 1980; 134:577-583.
[12] Erlemann R, Edel G, Roessner A et al. [Determination of the growth rate of tumor-like space-occupying lesions of the bones. A study of 1154 lesions of the long tubular bones]. Der Radiologe 1994; 34:53-58.
[13] Mankin HJ, Mankin CJ, Simon MA. The hazards of the biopsy, revisited. Members of the Musculoskeletal Tumor Society. The Journal of bone and joint surgery. American volume 1996; 78:656-663.
[14] Andreou D, Bielack SS, Carrle D et al. The influence of tumor- and treatment-related factors on the development of local recurrence in osteosarcoma after adequate surgery. An analysis of 1355 patients treated on neoadjuvant Cooperative Osteosarcoma Study Group protocols. Annals of oncology 2011: official journal of the European Society for Medical Oncology / ESMO 22:1228-1235.
[15] Holzapfel BM, Ludemann M, Holzapfel DE et al. [Open biopsy of bone and soft tissue tumors: guidelines for precise surgical procedures]. Operative Orthopadie und Traumatologie 2012; 24:403-415; quiz 416-407.
[16] Enneking WF, Spanier SS, Goodman MA. A System for the surgical staging of musculoskeletal sarcoma. Clin ORthop Rel Res 1980; 153: 106-120.
[17] Gradinger R, Rechl H, Hipp E. Pelvic osteosarcoma. Resection, reconstruction, local control and survival statistics. Clin Orthop Relat Res 1991; 270:149-158.
[18] Hogendoorn PC. ESMO/EUROBONET Working Group Bone Sarcomas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2010; 21(Suppl 5): 204-213.
Vor Biopsie einer ossären Läsion sollte das lokale Staging durch Abbildung des gesamten Knochens mit angrenzenden Gelenken und umgebenden Kompartimenten abgeschlossen sein.