01.04.2026 Thoraxchirurgie
Pneumothorax – aktuelles Management im chirurgischen Fokus
Ein Pneumothorax (PT) beschreibt die pathologische Ansammlung von Luft zwischen Pleura visceralis und parietalis, die durch Verletzung der Lunge oder des Brustkorbs auftritt. Bei Entwicklung eines Ventilmechanismus kann ein Spannungspneumothorax entstehen. Durch Mediastinalshift und vermindertem venösen Rückstrom kann sich eine akut lebensbedrohliche Situation entwickeln, die eine sofortige Entlastung erfordert. Ätiologisch werden spontane Pneumothoraces (SP) von erworbenen Formen (iatrogen, traumatisch) abgegrenzt. Eine Unterteilung zeigt Abbildung 1A, PT im Kindesalter werden in diesem Artikel nicht behandelt. Der SP zeigt eine zweigipflige Altersverteilung mit Häufung im 15.-30. Lebensjahr sowie im höheren Lebensalter > 60 Jahre [13]. Klinisch wird zwischen primärem Spontanpneumothorax (PSP, ohne klinisch manifeste Grunderkrankung) und sekundärem Spontanpneumothorax (SSP) (mit zugrundeliegender Lungenerkrankung) unterschieden [29].
Pathophysiologisch werden beim SP häufig emphysematöse, subpleurale Blebs und Bullae vorgefunden, die nicht immer nachzuweisen sind (Abb. 2 [26]). Neben der Ruptur makroskopischer Veränderungen wird eine diffus erhöhte Porosität der viszeralen Pleura vermutet, die auch makroskopisch unauffällige Areale betreffen kann. Diese wenige Mikrometer messenden Defekte der Pleura viszeralis ermöglicht den Austritt alveolärer Luft in den Pleuraspalt [3, 29].
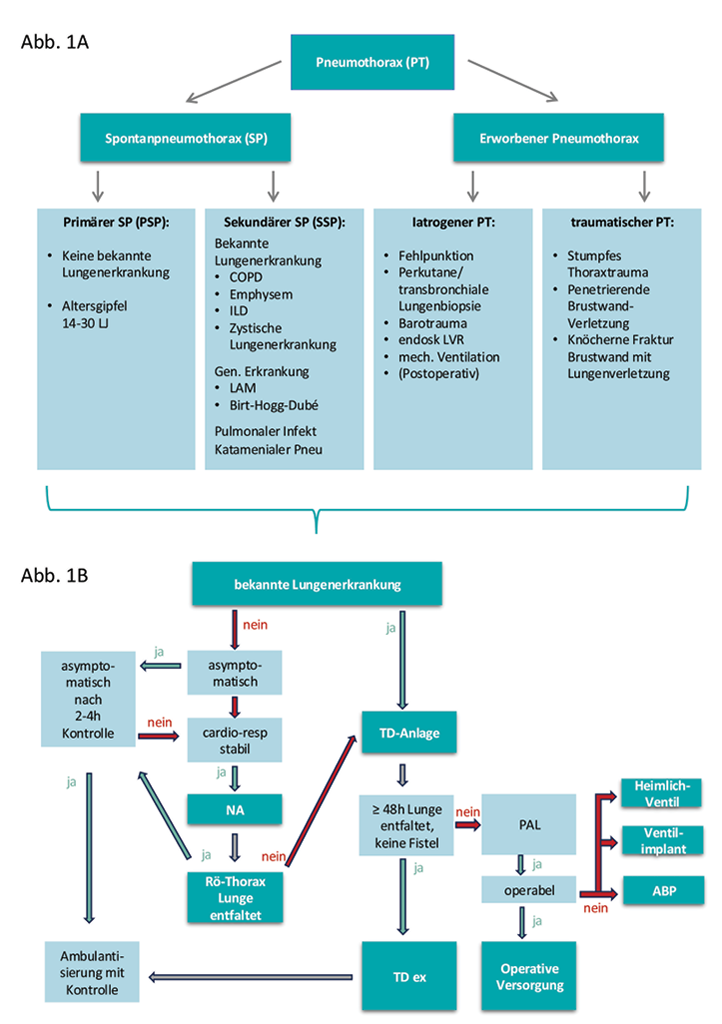
Abb.1A: Unterteilung des Pneumothorax
Abb. 1B: Handlungspfad der Autoren zum PT, der in Anlehnung an die BTS-Guidelines für SP [38]
auch für iatrogene PT und mit Einschränkung der NA bei traumatischem PT angewandt werden kann.
Diagnostik
Die klinische Symptomatik besteht häufig aus akutem thorakalem, einseitigem, stechendem Schmerz, der sich durch tiefes Einatmen verstärkt und innerhalb 24h nachlässt [29], oft in Verbindung mit Dyspnoe, Husten, Zyanose und – bei Spannungskomponente – Zeichen der Kreislaufinstabilität. Nach Anamnese und klinischer Untersuchung (Auskultation, Atemfrequenz, Kreislaufparameter, periphere Sauerstoffsättigung) erfolgt die Diagnosesicherung in der Regel mittels Röntgen-Thorax p.-a. im Stehen. Die Röntgenaufnahme dient der Abschätzung des Ausmaßes, der Erfassung möglicher Grunderkrankungen und ggf. Kontrolle bei bereits liegender Thoraxdrainage (TD) [18]. Die Thoraxsonografie ermöglicht in geübter Hand eine rasche Diagnostik insbesondere bei liegenden oder kritisch kranken Patient:innen sowie bei thorakaler Intervention [16]. Eine Computertomographie ist bei unklarer Befundlage, atypischem Verlauf, Verdacht auf SSP oder zur präoperativen Beurteilung sinnvoll. Als Routinediagnostik beim Erst-PSP ist sie aufgrund Strahlenexposition und begrenzter Zusatzinformation nicht obligat [18, 20].

Abb. 2: Schematische Darstellung emphysematöser Lungenveränderungen beim PSP [26]
Akuttherapie
Aktuelle Leitlinien betonen, dass die Behandlung primär an klinischer Stabilität und Symptomlast ausgerichtet werden soll und nicht ausschließlich am radiologischen Ausmaß des PT [31, 38]. Bei minimal symptomatischen, klinisch stabilen PSP-Patient:innen (subjektive Dyspnoe ≤ 1/10; subj. Schmerz ≤ 2/10) kann nach Beobachtung (2–4 h) eine konservative Therapie mit Analgesie und engmaschiger ambulanter Kontrolle gewählt werden. In einer randomisierten Studie erreichten 84,6 % der konservativ behandelten Patient:innen ohne Intervention innerhalb von acht Wochen eine vollständige Reexpansion [5]. Dieses Vorgehen setzt eine verlässliche Nachsorgestruktur und Aufklärung über Warnzeichen eines Rezidivs (zunehmende Dyspnoe, Thoraxschmerz, Synkope), Kontaktwege sowie raschen Zugang zur klinischen Reevaluation voraus.
Bei symptomatischen, aber kardiorespiratorisch stabilen Patient:innen erfolgt primär eine aktive Luftableitung. Beim PSP wird die Nadelaspiration (NA) als gering invasives Verfahren empfohlen. Bei ausbleibendem Erfolg oder bei SSP ist eine TD erforderlich [31, 38]. Dem Patientenwille – insbesondere im Hinblick auf ambulante Behandlung – wird in den aktuellen Empfehlungen mehr Bedeutung zugemessen als dem radiologischen PT-Ausmaß, sofern die Patient:in klinisch stabil ist und die Versorgungsstrukturen dies erlauben [3, 20]. Bei geeigneter PSP-Patient:in kann eine ambulante Behandlung nach NA oder Therapie mit Minidrain/Heimlich-Ventil ausreichen, erfordert aber geplante klinische und bildgebende Kontrollen innerhalb von 24–72 h sowie klare Eskalationskriterien [14].
Bei instabiler Patient:in ist eine sofortige Entlastung und nachfolgende kontinuierliche Ableitung mittels TD indiziert – in der Notfallsituation auch vor vollständiger bildgebender Abklärung. Als Merkmale eines hohen Risikos gelten bekannte Lungenerkrankung, Komorbidität, beidseitige PT, Hypoxiämie, Spannungs- oder ein Hämatopneumothorax [18]. Grundsätzlich gilt: je ausgeprägter die Komorbidität und je geringer die respiratorische Reserve, desto niedriger ist die Schwelle zur stationären Behandlung und zur konsequenten Drainageführung.
Die Prinzipien der symptomorientierten Therapie lassen sich auf iatrogene PT (z. B. nach Punktion/Biopsie) übertragen. Beim traumatischen PT wird – neben dem kardiorespiratorischen Zustand – das Ausmaß berücksichtigt. Bei stabilen Patient:innen mit geringem PT kann eine engmaschig überwachte konservative Therapie vertretbar sein [4], während bei Instabilität oder relevantem PT eine TD-Anlage obligat ist [15].
Management der Thoraxdrainage
TD sind in unterschiedlichen Größen und Bauformen verfügbar, prinzipiell werden dick- und dünnlumige Drainagen (> 20Fr oder < 20Fr) unterschieden [9]. Für die reine Luftableitung eignen sich dünnlumige Katheter, die meist über Seldingertechnik oder sonographiegesteuerte Direktpunktion mit geringerem Trauma eingebracht werden und weniger Schmerzen verursachen [6; 24]. Limitationen sind ein höheres Risiko für Abknicken, Dislokation oder Obstruktion, insbesondere bei zähem Sekret oder Blut. Bei hohem Luftleckvolumen oder kombiniertem Flüssigkeits-/Blutanteil sind dicklumige Systeme funktionell überlegen, deren Anlage durch Finger-Thorakostomie sicher und gut zu platzieren ist. Die TD-Anlage in Trokartechnik soll bei erheblicher Verletzungsgefahr der Brustwand wie der thorakalen Organe vermieden werden [19]. Technische Aspekte der Drainageleistung folgen physikalischen Prinzipien (Hagen-Poiseuille), klinisch entscheidend bleiben jedoch Lage, Durchgängigkeit, Dichtigkeit des Systems und eine Beurteilung des Luftlecks [2, 9]. Digitale Drainagesysteme können die interindividuelle Variabilität der Luftleckbeurteilung reduzieren und die Mobilität verbessern. Evidenzbasierte Schwellenwerte für die Entfernung der TD bei PT liegen nicht vor. Bei ausgedehnter Lunge und Sistieren des Luftlecks sollte die Drainage nach 48 h entfernt werden, wobei die geförderte Flüssigkeit nicht blutig oder purulent und < 450 ml/24h sein soll [22].
Persistierendes Luftleck
Wird 48 h nach TD-Anlage bei PT eine Luftfistel nachgewiesen, spricht man von einer anhaltenden Lungenfistel (persisting/ongoing air leak, PAL) [31]. Dieser Begriff definiert ursprünglich ein persistierendes Leck ab dem 5–7 Tag nach größerer Lungenresektion und ist mit prolongierter Hospitalisation und erhöhter Morbidität verbunden [10; 11, 33]. Beim PSP kann ein Teil der Leckagen spontan sistieren, während beim SSP und bei ausgeprägter parenchymatöser Vorschädigung häufiger eine persistierende Fistel auftritt. Eine technische Undichtigkeit (System, TD-Eintrittstelle) sollte frühzeitig ausgeschlossen und interdisziplinär eine definitive Strategie festgelegt werden. Ist der Patient:in operabel, bleibt die operative Versorgung die beste definitive Therapieoption [30]. Bei fehlender Operabilität kommen endobronchiale Ventile als zugelassene Option in Betracht. Aufgrund kollateraler Ventilation [36] kann die Okklusion mehrerer Segmente erforderlich werden, was funktionell relevant sein kann [27]. Alternativ ist die autologe Blutpleurodese (ABP) eine pragmatische und kostengünstige Option. In Metaanalysen nach Lungenresektion werden hohe Erfolgsraten bei überschaubarem Komplikationsprofil beschrieben [21]. Ein Entscheidungspfad der Autoren in Anlehnung an die BTS-Guideline [38] ist in Abb. 1B angeführt, der auch für erworbene PT angewandt werden kann.
Operative Therapie und Rezidivprophylaxe
Aus chirurgischer Sicht hat die operative Therapie beim Pneumothorax einen hohen Stellenwert, insbesondere bei persistierendem Luftleck, bilateralem Ereignis, SpannungsPT, Rezidiv, Berufsrisiko (z. B. Pilot:in, Taucher:in) oder bei Patient:innen, die eine maximale Rezidivprävention priorisieren. Die videoassistierte Thorakoskopie mit Resektion des pathologietragenden Lungengewebes (Keilresektion/Bullektomie) stellt die Standardtherapie dar [30]. Ergänzend kann eine mechanische Pleurodese (Pleurektomie, Abrasion) oder chemische Pleurodese (z. B. Talkum, Minocyclin) durchgeführt werden. In systematischen Übersichten werden sehr niedrige Rezidivraten nach additiver Pleurodese berichtet [16]. Gleichzeitig bleibt die optimale Kombination aus Resektion und Pleurodesetechnik Gegenstand laufender Studien, da einzelne Arbeiten keinen zusätzlichen Vorteil einer mechanischer Pleurodese gegenüber der Resektion allein zeigen, während andere Daten eine additive Pleurodese nahelegen [3; 28, 31].
Rezidivrisiko
Nach konservativer Erstbehandlung eines PSP werden Rezidivraten von etwa 32 % beschrieben, wobei der größte Anteil innerhalb des ersten Jahres auftritt [37]. Dies ist für die Patientenaufklärung relevant und erklärt, weshalb Leitlinien bei bestimmten Konstellationen (z. B. Berufsrisiko oder hohe Präferenz für Rezidivvermeidung) bereits bei der Erstmanifestation eine operative Therapie diskutieren [37; 38]. Mechanische Pleurodeseverfahren wie Abrasion oder Pleurektomie zeigen in Metaanalysen vergleichbare Rezidivraten unter 4 %, unterscheiden sich jedoch in perioperativer Belastung (Krankenhaus-, Drainagedauer, Blutverlust) zugunsten der Abrasion [6]. Chemische Pleurodesen reduzieren das Rezidivrisiko weiter auf 1,2 % [34], wobei die Langzeitwirkung etwa von Talkum nicht berücksichtigt wird. In der Praxis sollte die Wahl der Technik an Erfahrung des Teams, Risikoprofil und dem erforderlichen Grad der Rezidivprävention ausgerichtet werden.
Lebensführung und Beratung
Ein Pneumothorax ist für viele Patient:innen ein einschneidendes Ereignis und bietet die Gelegenheit, Risikofaktoren konsequent zu adressieren. Tabakrauchen erhöht das Risiko für SP und Rezidive, die Raucherentwöhnung ist eine zentrale Präventionsmaßnahme [7, 37]. Zusätzlich ist insbesondere die kombinierte Inhalation von Tabak und Cannabis mit einem erhöhten Risiko für PSP und bullöse Veränderungen assoziiert [17; 35].
Die Nutzung kommerzieller Flugzeuge ist nach radiologisch bestätigter vollständiger Reexpansion in der Regel nach sieben Tagen möglich [8]. Tauchen mit Druckluft ist nach Pneumothorax nur nach gesicherter Rezidivprävention – zumeist operativ – und qualifizierter Tauchtauglichkeitsprüfung zu empfehlen [12]. Die Atemschutztauglichkeit bei Feuerwehren kann erst nach radiologisch bestätigter Abheilungslatenz von sechs Wochen im Rahmen einer DGUV G26-Untersuchung erteilt werden.
Bei Frauen im gebärfähigen Alter muss der katameniale Pneumothorax differentialdiagnostisch in Betracht gezogen werden. Er tritt zum Einsetzen der Menstruation auf, wird aufgrund fehlender Anamnese oft verkannt [1] und geht mit einer hohen Rezidivrate einher [32]. Pathognomonisch sind Zwerchfelllücken und pleurale Endometrioseherde [23, 25]. Die Identifikation betroffener Patientinnen ist wichtig, da die alleinige chirurgische Behandlung zur Rezidivprophylaxe nicht ausreichend ist und durch hormonelle Therapie in Anlehnung an die Endometriosebehandlung flankiert werden muss [25, 32].
Zusammenfassung
Der Pneumothorax erfordert eine individualisierte, symptomorientierte Therapie. Beim minimal symptomatischen PSP ist ein konservatives Vorgehen mit strukturierter ambulanter Kontrolle evidenzbasiert möglich. Gleichzeitig verbleibt die chirurgische Therapie bei Rezidiv oder persistierendem Luftleck das definitive Verfahren der Wahl. Der klinische Schlüssel liegt in der passgenauen Auswahl der Therapie unter Berücksichtigung von Stabilität, Grunderkrankung, Versorgungsstruktur und dem informierten Willen der Patient:in.
Die Literaturliste erhalten Sie auf Anfrage via passion_chirurgie@bdc.de.

Korrespondierender Autor:
Dr. med. Cosmas D. Wimmer
Klinik für Thoraxchirurgie
Thoraxklinik des Universitätsklinikum Heidelberg
cosmas.wimmer@med.uni-heidelberg.de

Dr. med. Henrike Deißner
Klinik für Thoraxchirurgie
Thoraxklinik des Universitätsklinikum Heidelberg
Chirurgie
Wimmer CD, Deißner H: Pneumothorax – aktuelles Management im chirurgischen Fokus. Passion Chirurgie. 2026 April; 16(04): Artikel 03_03.
Weitere aktuelle Artikel
18.09.2017 Fachgebiete
Präoperative Evaluation erwachsener Patienten vor elektiven, nicht herz-thoraxchirurgischen Eingriffen
Die vorliegenden Empfehlungen gelten für erwachsene Patienten vor elektiven, nicht kardiochirurgischen und nicht lungenresezierenden Eingriffen. Es handelt sich um eine Überarbeitung und Aktualisierung der erstmals im Jahre 2010 publizierten Empfehlungen der Deutschen Fachgesellschaften der Inneren Medizin, Chirurgie und Anästhesiologie [1], die seither im deutschsprachigen Raum eine gute Durchdringung und Akzeptanz erfahren haben [2,3].
09.08.2016 BDC|News
Reisestipendien für Studenten zum DGT-Kongress
In diesem Jahr vergibt die Deutsche Gesellschaft für Thoraxchirurgie (DGT) erstmalig zehn Reisestipendien für Studenten zur Teilnahme an der Jahrestagung in Freiburg im Wert von 250 Euro. Bewerbungsschluss ist am 04. September 2016.
24.02.2016 Thoraxchirurgie
Gesamtzahl der herzchirurgischen Eingriffe auf stabilem Niveau
Fachgesellschaft der deutschen Herzchirurgen veröffentlicht DGTHG-Leistungsstatistik 2015: trotz höherem Durchschnittsalter der Patienten bessere Überlebensraten
12.02.2016 Thoraxchirurgie
Herausforderung Mesotheliom
Das maligne Pleuramesotheliom (MPM) ist ein bösartiger Tumor, der von
Lesen Sie PASSION CHIRURGIE!
Die Monatsausgaben der Mitgliederzeitschrift können Sie als eMagazin online lesen.